特定使用成績調査 -非がん性慢性疼痛患者を対象とした長期使用に関する調査- <最終報告>
「禁忌を含む注意事項等情報」等につきましては電子添文情報をご参照ください。
調査の概要
- 調査目的
-
オピオイド誘発性便秘症を有する非がん性慢性疼痛患者に対するスインプロイク錠(以下、本剤)の長期使用時を含む使用実態下における安全性及び有効性に関する情報を収集する。また、本剤の重要な特定されたリスクである下痢が発現、あるいは重篤化しやすい患者背景の探索を行うことを目的とする。
- 調査対象
-
本剤の使用経験のないオピオイド誘発性便秘症を有する非がん性慢性疼痛患者
- 収集症例数
-
351例
- 実施施設数
-
74施設
- 調査方法
-
中央登録方式
- 調査実施期間
-
2018年1月~2022年3月
- 観察期間
-
本剤の投与開始から最長52週間(52週間未満の場合、投与終了日まで)
- 解析対象症例
-
安全性解析対象症例:348例、有効性解析対象症例:303例
- 調査実施者
-
塩野義製薬株式会社及びシオノギファーマコビジランスセンター株式会社
- 本報告の限界
-
・本調査はコントロール群のない観察研究である。
・有効性の結果には患者からの自己申告に基づくため想起バイアスが含まれる可能性が否定できない。
・患者背景因子や治療因子、時点ごとの結果について例数の偏りによる影響があった可能性を否定できない。
・本邦のみの調査であることから、人種差等の観点から本結果の一般化には一部限界がある。
- 安全性調査事項
-
下痢、オピオイド離脱症候群及びオピオイドの鎮痛効果の減弱の他、臨床検査値の異常変動を含むその他の事象の発現状況を調査した。なお、便秘症状の増悪は有害事象としなかった。有害事象のうち、本剤との因果関係が否定できない事象を副作用とし、ICH 国際医薬用語集日本語版(MedDRA/J Ver. 24.1)に基づき集計した。また、患者背景因子別及び治療因子別の上記発現状況についても検討した。
- 有効性調査事項
-
本剤投与開始2週後、4週後、8週後、12週後、24週後、36週後、52週後の各観察時点で本剤が投与中かつ各改善度が評価されていた症例を対象とした。該当症例について、各観察時点又は投与中止・終了時の排便回数の改善度(「改善」「不変」「悪化」症例に対する「改善」症例の割合)及び排便状況(便の硬さ、いきみ、残便感)の改善度(「改善」「やや改善」「不変」「やや悪化」「悪化」症例に対する「改善」「やや改善」症例の割合)を調査した。また、患者背景因子別、治療因子別の上記改善割合についても検討した。
- 統計解析
-
統計解析にはSAS® Release 9.2以上(SAS Institute Inc., Cary, NC, USA)を用いた。検定の有意水準は両側5%、信頼区間は両側95%とした。
【安全性】副作用の発現例数を集計し発現割合を算出した。
・安全性に影響を与える要因の探索では、「不明」のカテゴリの症例を除き、カテゴリ間の独立性の評価にはカイ2乗検定、順序カテゴリに伴う傾向性の評価にはCochran-Armitage検定を用い、傾向性の適合度検定も実施した。
・要因分析には独立性の評価で有意になった因子を説明変数とした多変量ロジスティック回帰モデルを適用した。
要因分析では、本剤投与に関する項目及び併用薬に関する項目については有意差がみられた場合も説明変数として採用しなかった。
【有効性】排便回数及び排便状況について、各観察時点で本剤が投与中であり、かつ改善度が評価されている症例における改善割合を算出した。
・有効性に影響を与える要因の探索では、「不明」のカテゴリの症例を除き、カテゴリ間の独立性の評価にはカイ2乗検定、順序カテゴリに伴う傾向性の評価にはCochran-Armitage検定を用い、傾向性の適合度検定も実施した。
・要因分析には独立性の評価で有意になった因子を説明変数とした多変量ロジスティック回帰モデルを適用した。
要因分析では、本剤投与に関する項目及び併用薬に関する項目については有意差がみられた場合も説明変数として採用しなかった。
納谷憲幸,他.新薬と臨牀.2023;72:201-31.を参考に作成
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
患者背景因子別症例分布
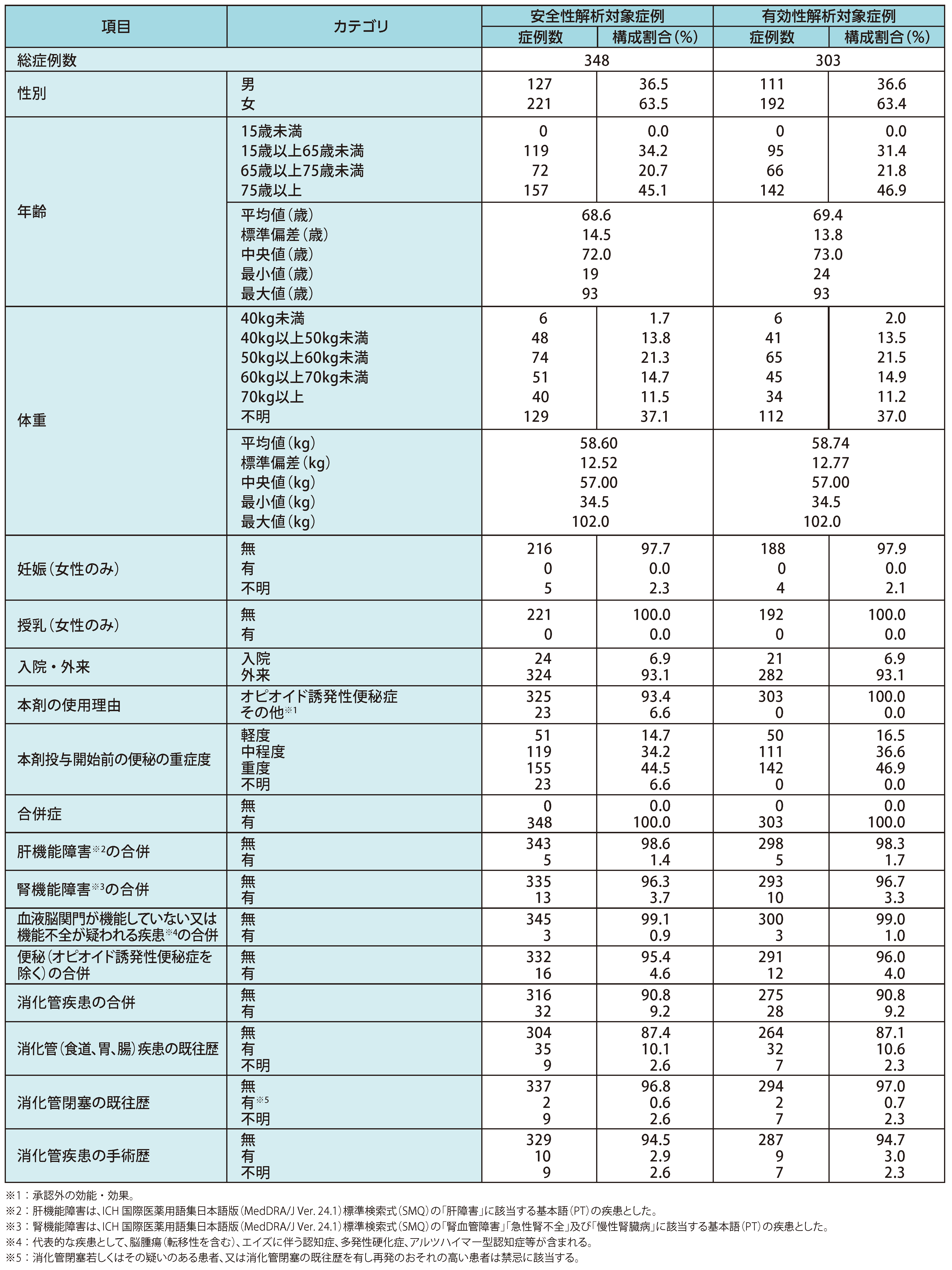
納谷憲幸,他.新薬と臨牀.2023;72:205-6.
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の禁忌(抜粋)】
2. 禁忌(次の患者には投与しないこと)
2.2 消化管閉塞若しくはその疑いのある患者、又は消化管閉塞の既往歴を有し再発のおそれの高い患者[消化管穿孔を起こすおそれがある。]
【スインプロイク錠の効能・効果、特定の背景を有する患者に関する注意(抜粋)】
4. 効能・効果
オピオイド誘発性便秘症
9. 特定の背景を有する患者に関する注意(抜粋)
9.1 合併症・既往歴等のある患者
9.1.2 血液脳関門が機能していない又は機能不全が疑われる患者
脳腫瘍(転移性を含む)などの患者では、オピオイド離脱症候群又はオピオイドの鎮痛作用の減弱を起こすおそれがある。[8.2 参照]
治療因子別症例分布
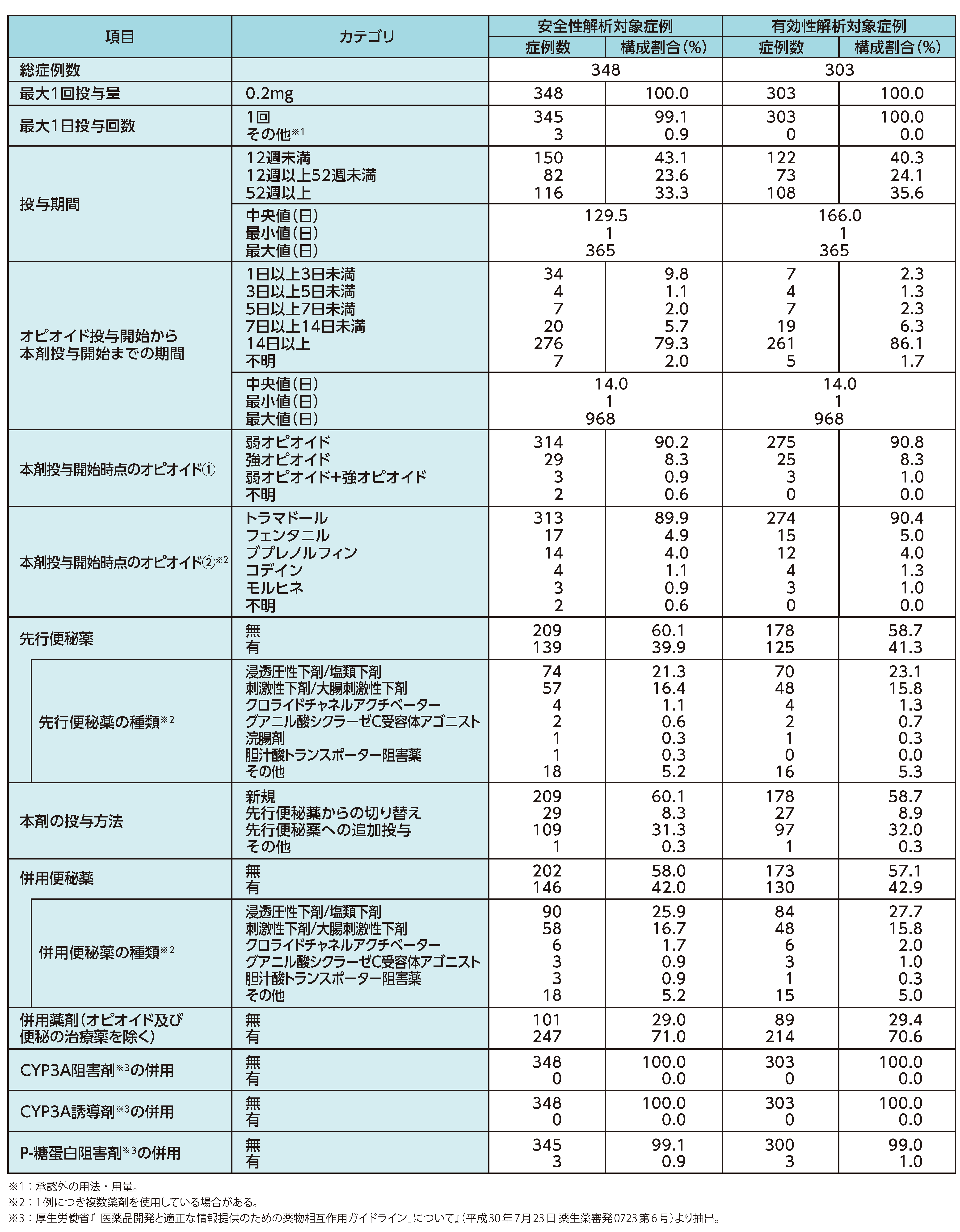
納谷憲幸,他.新薬と臨牀.2023;72:207-8.
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の用法・用量、相互作用(併用注意)】
6. 用法・用量
通常、成人にはナルデメジンとして1回0.2mgを1日1回経口投与する。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| CYP3A阻害剤 イトラコナゾール、フルコナゾール等 [16.7.4、16.7.5参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。 | CYP3A4を介する本剤の代謝が阻害される。 |
| CYP3A誘導剤 リファンピシン等[16.7.3参照] |
本剤の血中濃度が低下し、効果が減弱するおそれがある。 | CYP3A4を介する本剤の代謝が促進される。 |
| P-糖蛋白阻害剤 シクロスポリン等[16.7.2参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。また、血液脳関門への影響により、本剤の脳内濃度が上昇するおそれがある。 | P-糖蛋白を介する本剤の輸送が阻害される。 |
投与期間別の継続割合及び中止・終了理由の内訳と分布
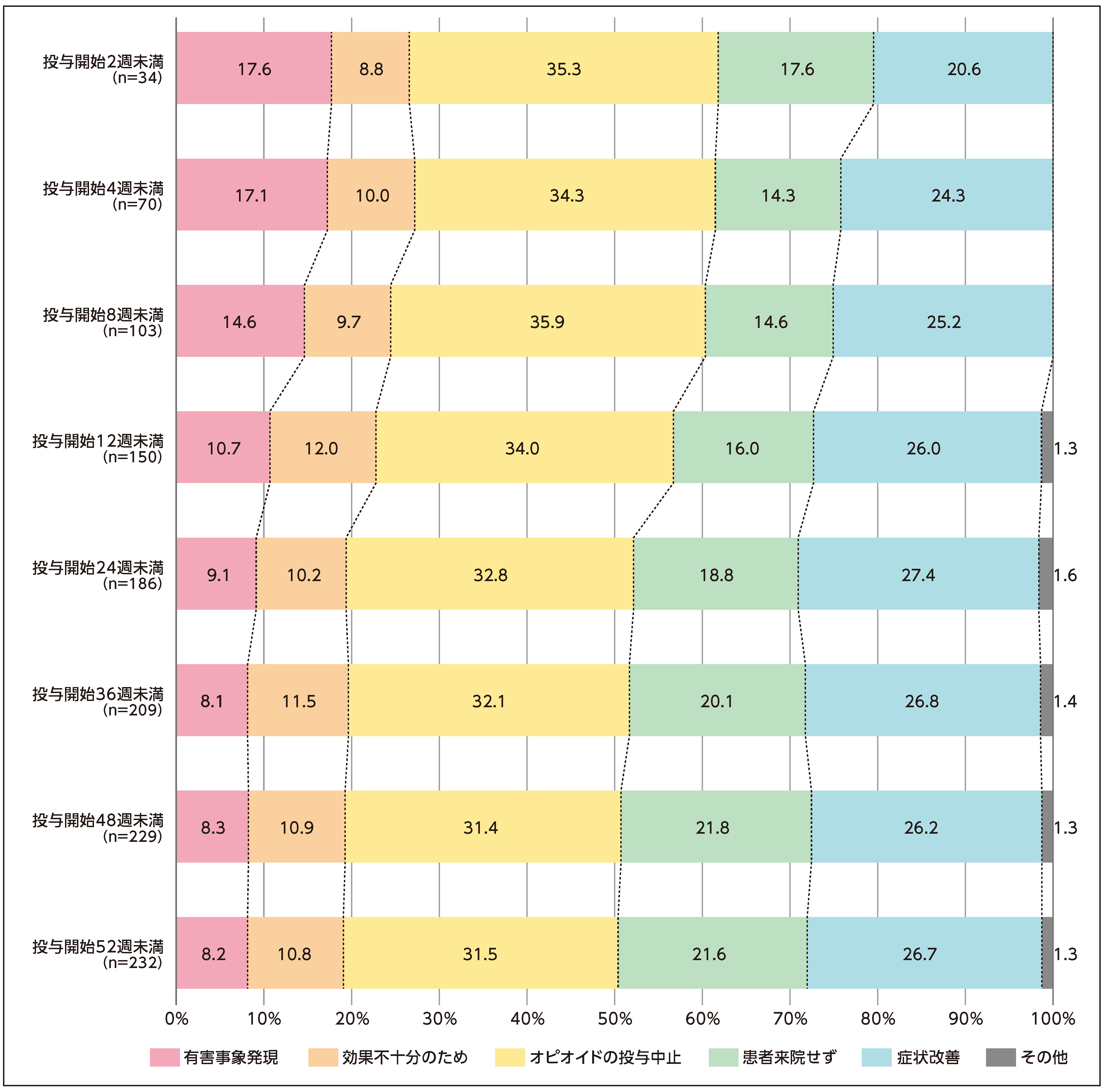
納谷憲幸,他.新薬と臨牀.2023;72:209.より作図
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
安全性 ◆副作用の発現状況(症例ごと)
安全性解析対象症例348例において、 副作用は21例に認められ、 副作用発現割合は6.03%でした。
副作用は下痢が14例(4.02%)と最も多く、次いで腹痛が6例(1.72%)、高血圧及び便意切迫、排便回数増加、悪心、口腔内不快感、軟便、頻尿、血中クレアチンホスホキナーゼ増加がそれぞれ1例(0.29%)でした。
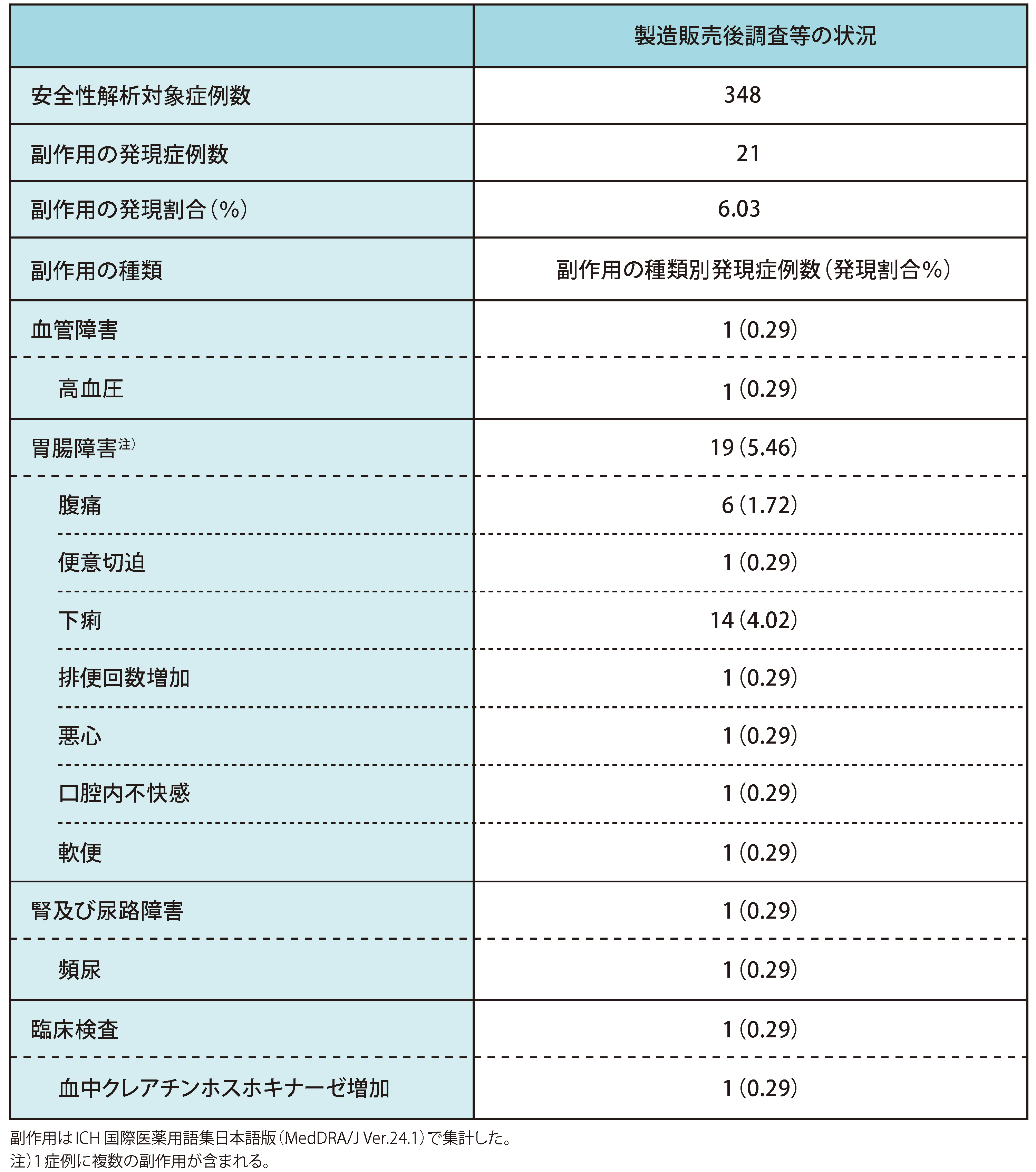
納谷憲幸,他.新薬と臨牀.2023;72:210.
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
安全性 ◆副作用の重篤性・発現時期・転帰
安全性解析対象症例348例のうち、副作用は21例において28件に発現し、 死亡等の重篤な副作用の発現はありませんでした。
発現時期は、 副作用28件のうち、本剤投与開始から1週未満が13件(46.4%)、 1週以上2週未満が5件(17.9%)、 2週以上4週未満が4件(14.3%)、 4週以上6週未満が2件(7.1%)、 8週以上が4件(14.3%)でした。
転帰は、回復又は軽快が25件(89.3%)、 未回復が3件注)(10.7%)でした。
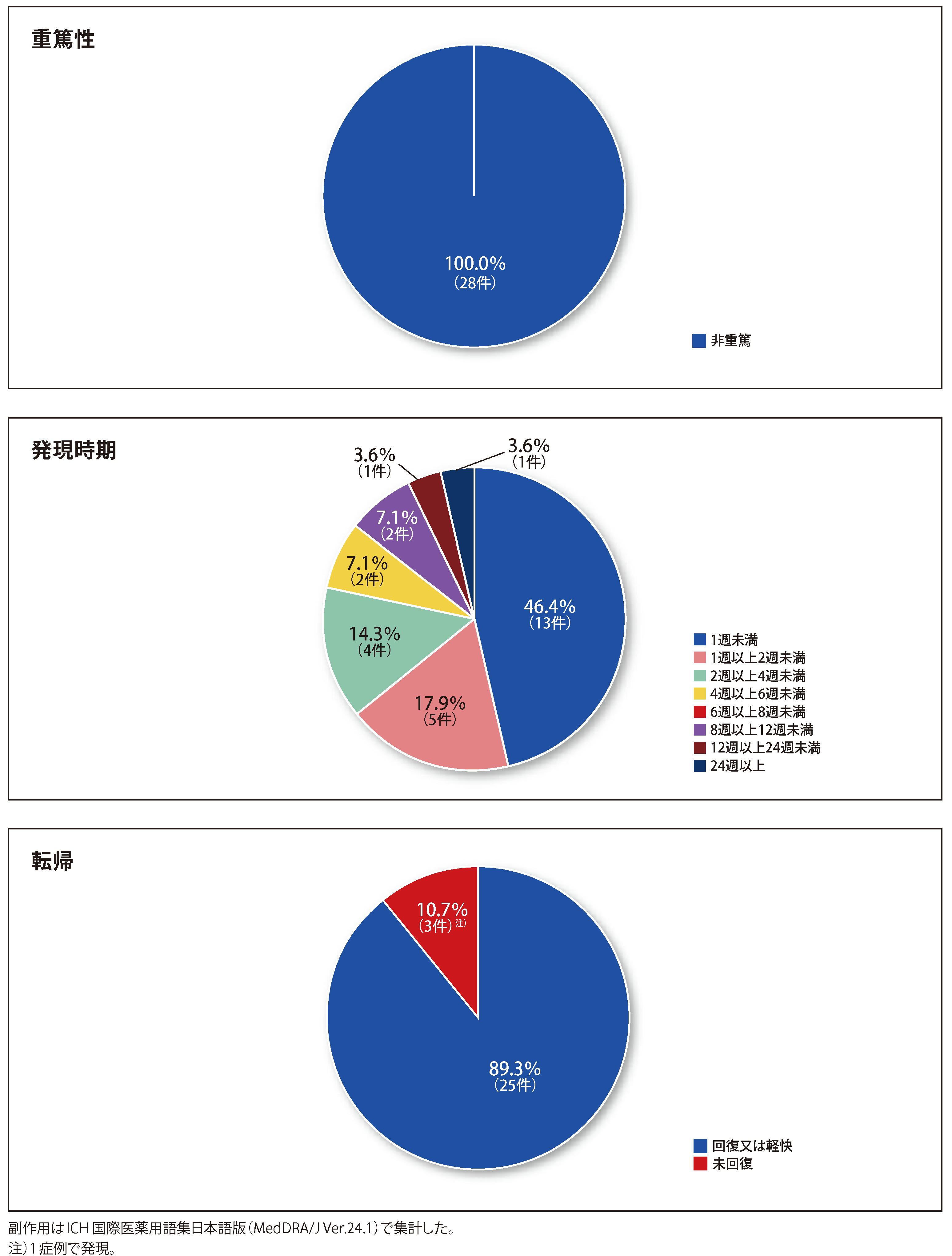
納谷憲幸,他.新薬と臨牀.2023;72:211.より作図
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
安全性 ◆下痢の重篤性・発現時期・転帰
安全性解析対象症例348例において、 下痢は14例(4.02%)に14件発現し、すべて非重篤でした。
発現時期は、 下痢14件のうち、本剤投与開始から1週未満が7件(50.0%)、 1週以上2週未満が1件(7.1%)、 2週以上4週未満が2件(14.3%)、 4週以上6週未満が1件(7.1%)、8週以上が3件(21.4%)でした。
転帰は、 全例が回復又は軽快でした。
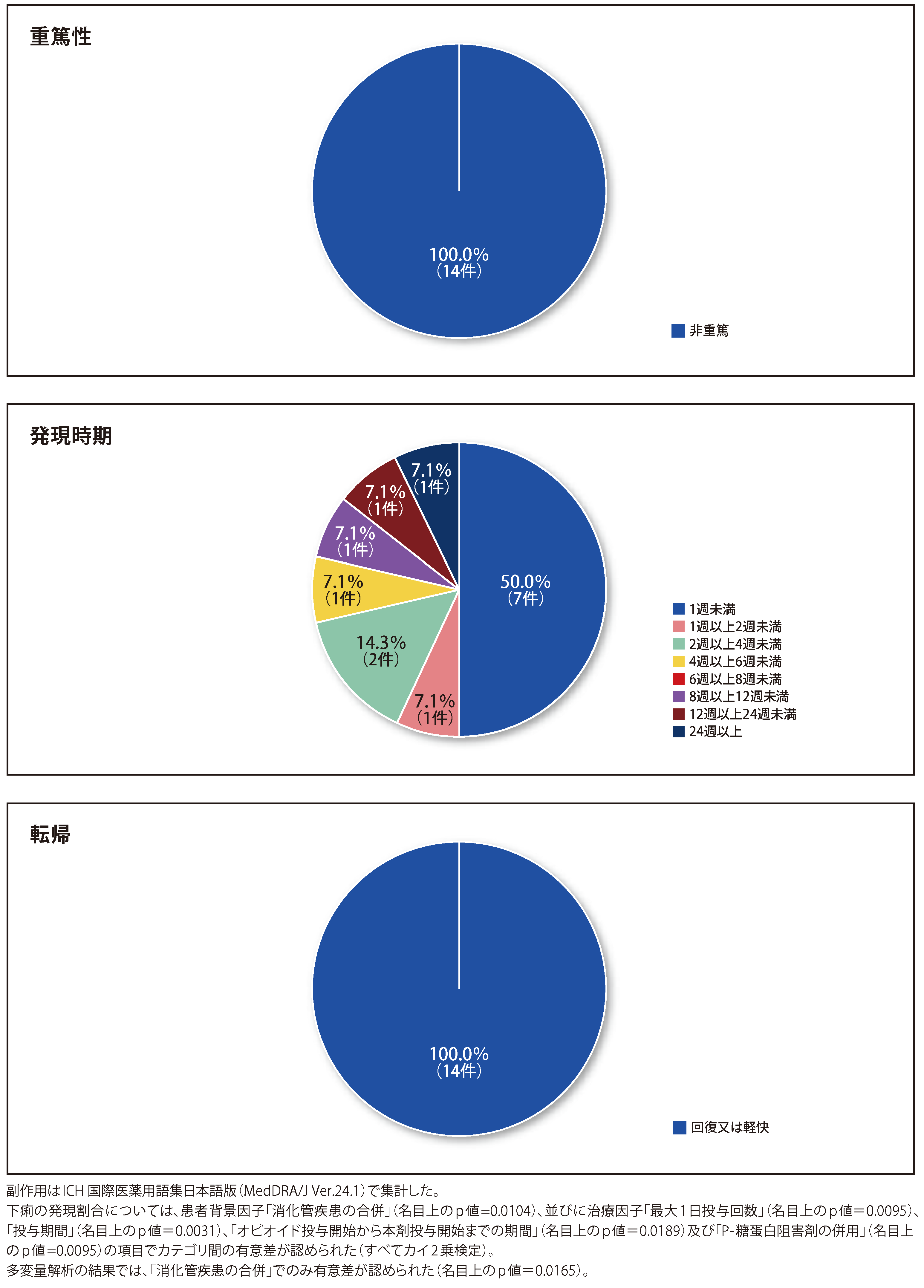
納谷憲幸,他.新薬と臨牀.2023;72:211.より作図
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
安全性 ◆患者背景因子別の副作用発現割合(サブグループ解析)
年齢別での副作用発現割合は、 15歳以上65歳未満(119例)で6.72%(8例)、 65歳以上75歳未満(72例)で12.50%(9例)、 75歳以上(157例)で2.55%(4例)でした。
また、 下痢の発現割合は15歳以上65歳未満で4.20%(5例)、 65歳以上75歳未満で6.94%(5例)、 75歳以上で2.55%(4例)でした。
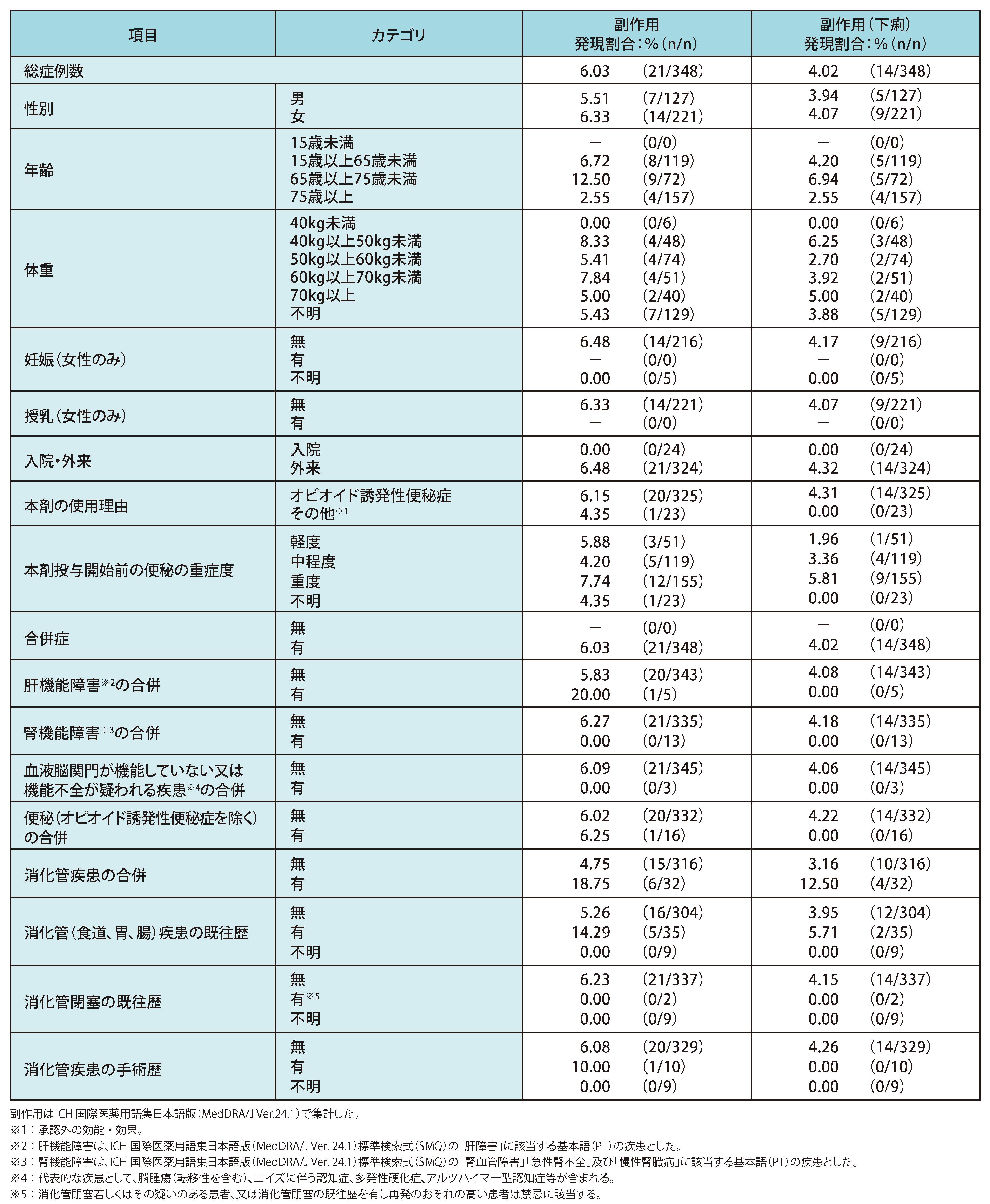
納谷憲幸,他.新薬と臨牀.2023;72:213-4.
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の禁忌(抜粋)】
2. 禁忌(次の患者には投与しないこと)
2.2 消化管閉塞若しくはその疑いのある患者、又は消化管閉塞の既往歴を有し再発のおそれの高い患者[消化管穿孔を起こすおそれがある。]
【スインプロイク錠の効能・効果、特定の背景を有する患者に関する注意(抜粋)】
4. 効能・効果
オピオイド誘発性便秘症
9. 特定の背景を有する患者に関する注意(抜粋)
9.1 合併症・既往歴等のある患者
9.1.2 血液脳関門が機能していない又は機能不全が疑われる患者
脳腫瘍(転移性を含む)などの患者では、オピオイド離脱症候群又はオピオイドの鎮痛作用の減弱を起こすおそれがある。[8.2 参照]
安全性 ◆治療因子別の副作用発現割合(サブグループ解析)
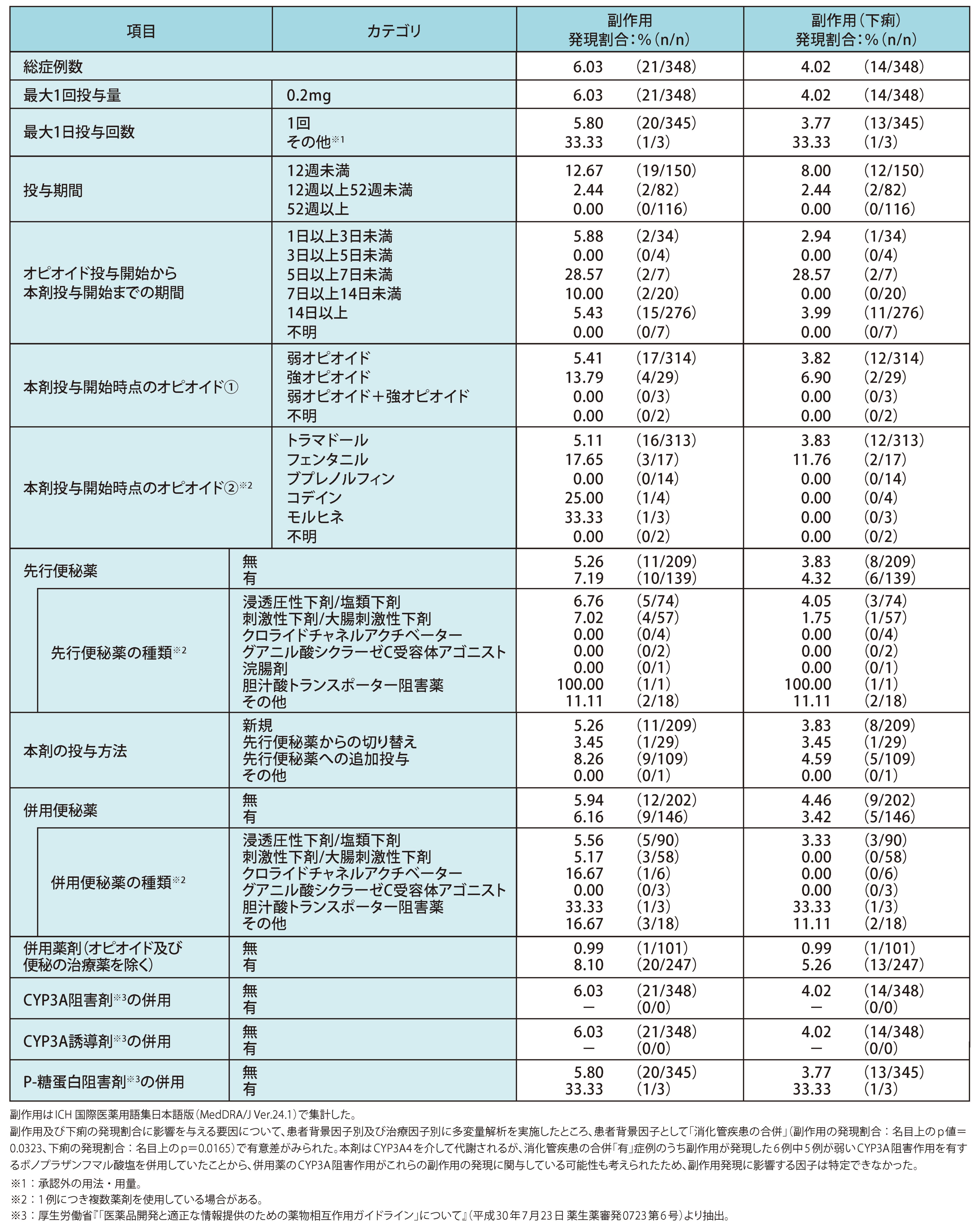
納谷憲幸,他.新薬と臨牀.2023;72:215-6.
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の用法・用量、相互作用(併用注意)】
6. 用法・用量
通常、成人にはナルデメジンとして1回0.2mgを1日1回経口投与する。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| CYP3A阻害剤 イトラコナゾール、フルコナゾール等 [16.7.4、16.7.5参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。 | CYP3A4を介する本剤の代謝が阻害される。 |
| CYP3A誘導剤 リファンピシン等[16.7.3参照] |
本剤の血中濃度が低下し、効果が減弱するおそれがある。 | CYP3A4を介する本剤の代謝が促進される。 |
| P-糖蛋白阻害剤 シクロスポリン等[16.7.2参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。また、血液脳関門への影響により、本剤の脳内濃度が上昇するおそれがある。 | P-糖蛋白を介する本剤の輸送が阻害される。 |
有効性 ◆排便回数及び排便状況の改善割合
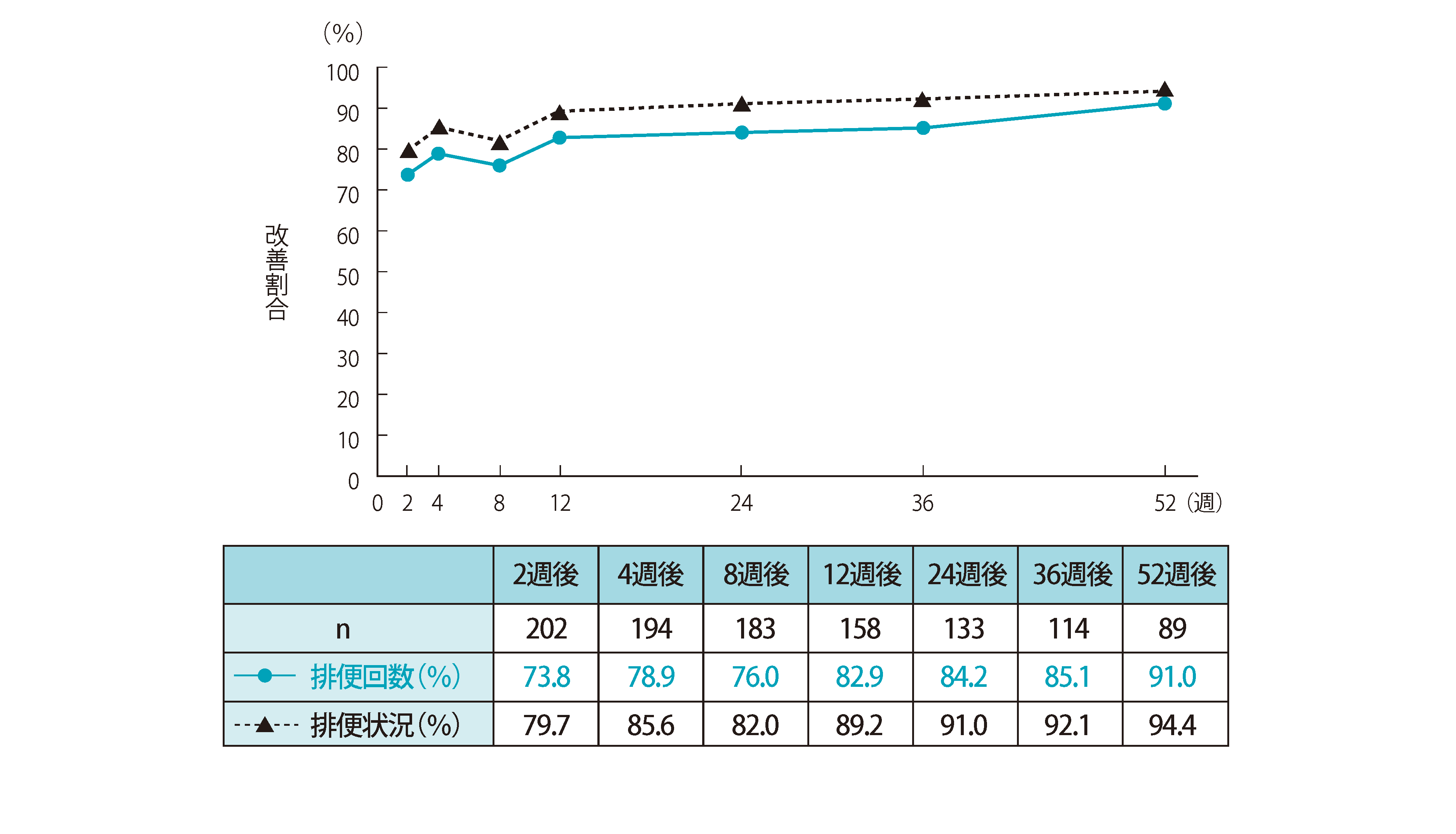
納谷憲幸,他.新薬と臨牀.2023;72:217.
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
有効性 ◆患者背景因子別の排便回数の改善割合(サブグループ解析)
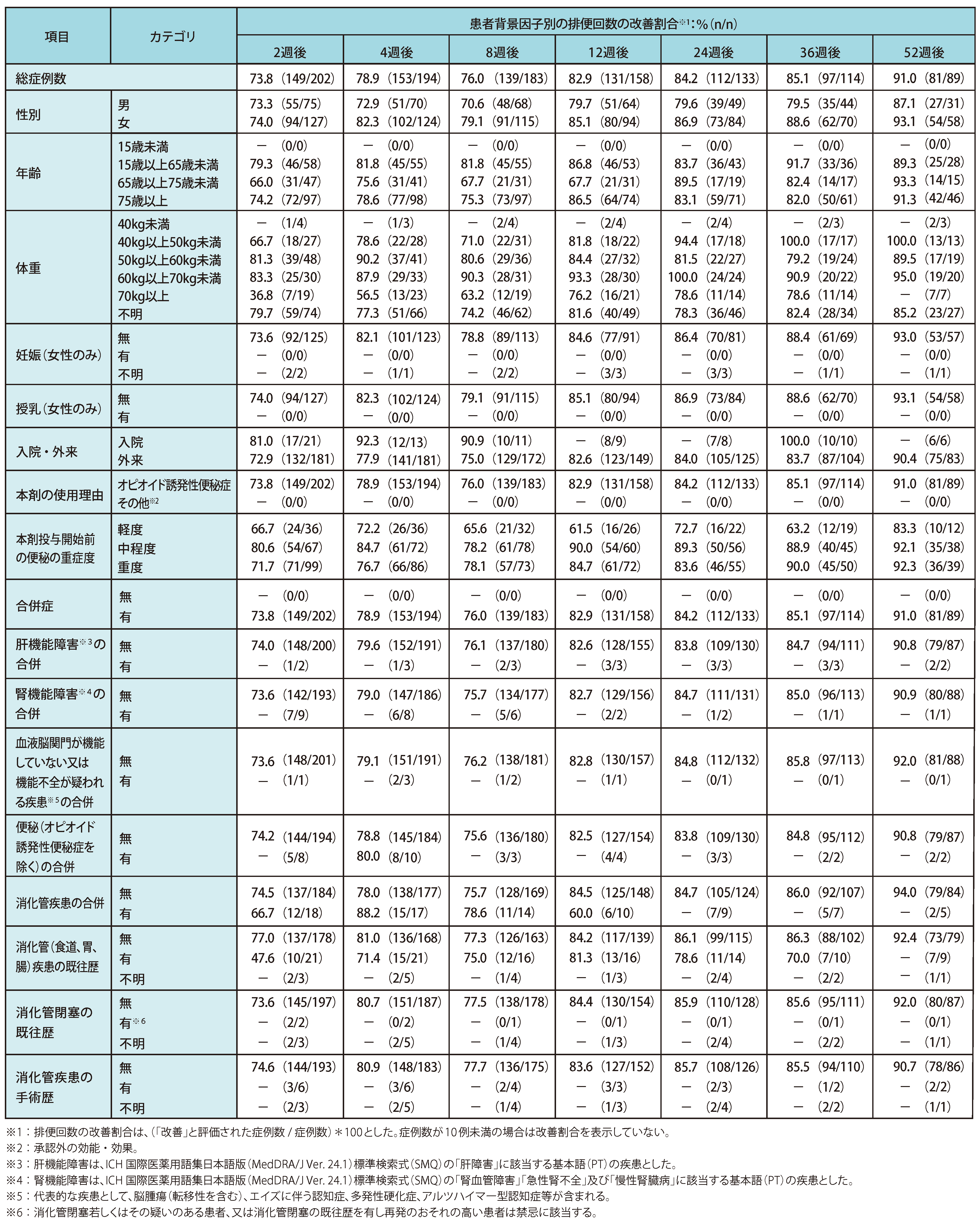
納谷憲幸,他.新薬と臨牀.2023;72:218-21.より作表
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の禁忌(抜粋)】
2. 禁忌(次の患者には投与しないこと)
2.2 消化管閉塞若しくはその疑いのある患者、又は消化管閉塞の既往歴を有し再発のおそれの高い患者[消化管穿孔を起こすおそれがある。]
【スインプロイク錠の特定の背景を有する患者に関する注意(抜粋)】
9. 特定の背景を有する患者に関する注意(抜粋)
9.1 合併症・既往歴等のある患者
9.1.2 血液脳関門が機能していない又は機能不全が疑われる患者
脳腫瘍(転移性を含む)などの患者では、オピオイド離脱症候群又はオピオイドの鎮痛作用の減弱を起こすおそれがある。[8.2 参照]
有効性 ◆患者背景因子別の排便状況の改善割合(サブグループ解析)
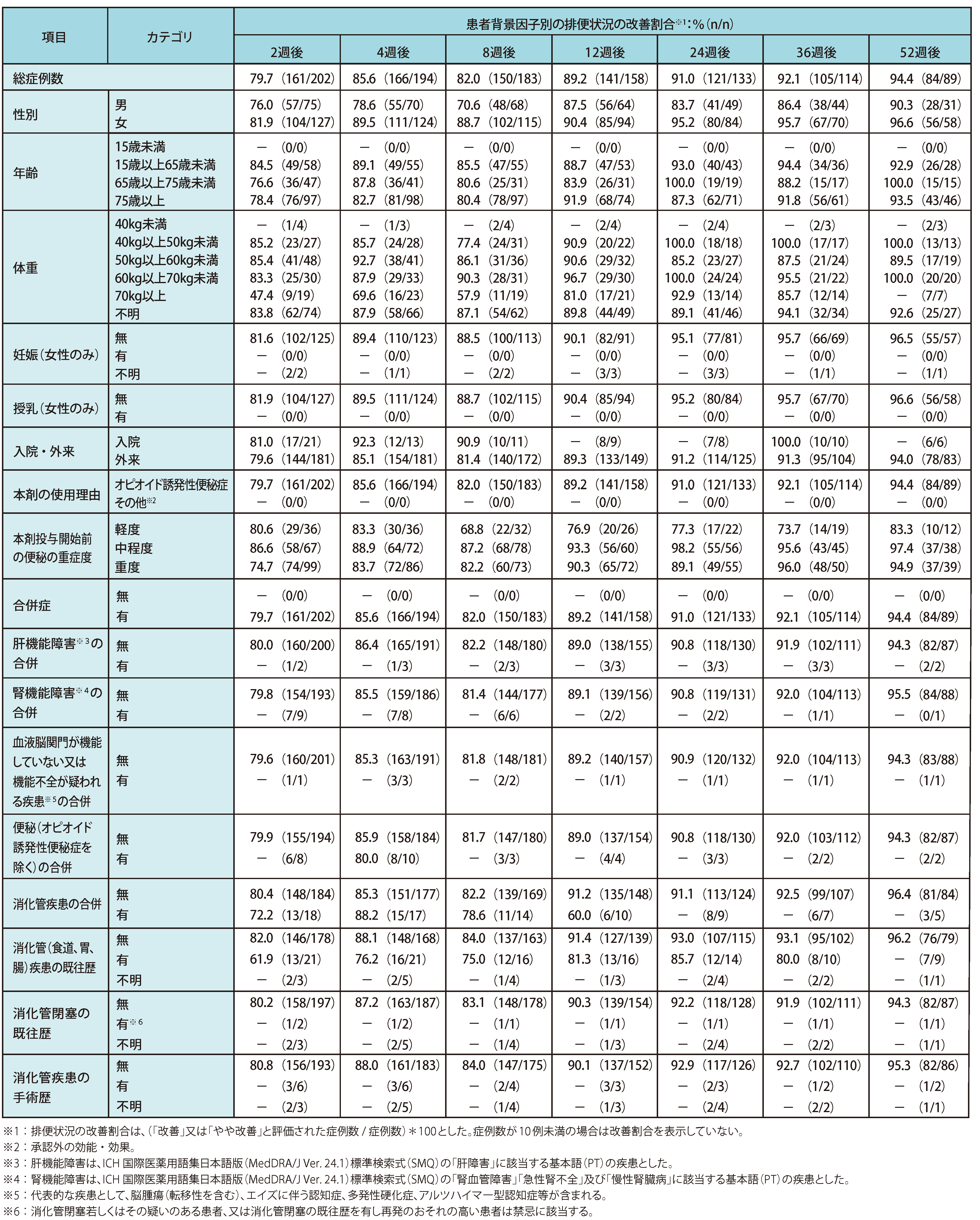
納谷憲幸,他.新薬と臨牀.2023;72:222-5.より作表
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の禁忌(抜粋)】
2. 禁忌(次の患者には投与しないこと)
2.2 消化管閉塞若しくはその疑いのある患者、又は消化管閉塞の既往歴を有し再発のおそれの高い患者[消化管穿孔を起こすおそれがある。]
【スインプロイク錠の特定の背景を有する患者に関する注意(抜粋)】
9. 特定の背景を有する患者に関する注意(抜粋)
9.1 合併症・既往歴等のある患者
9.1.2 血液脳関門が機能していない又は機能不全が疑われる患者
脳腫瘍(転移性を含む)などの患者では、オピオイド離脱症候群又はオピオイドの鎮痛作用の減弱を起こすおそれがある。[8.2 参照]
有効性 ◆治療因子別の排便回数の改善割合(サブグループ解析)
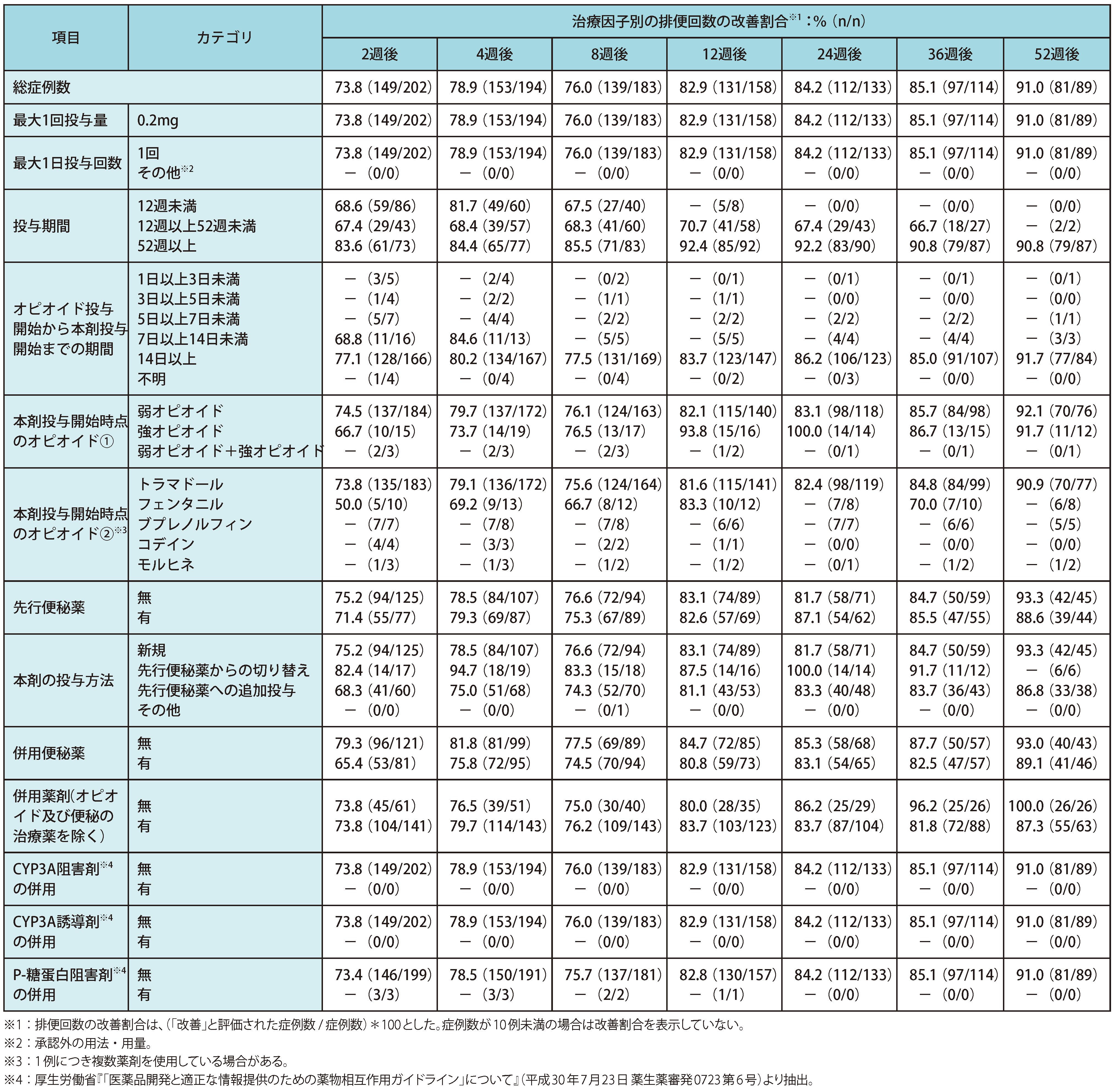
納谷憲幸,他.新薬と臨牀.2023;72:226-7.より作表
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の相互作用(併用注意)】
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| CYP3A阻害剤 イトラコナゾール、フルコナゾール等 [16.7.4、16.7.5参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。 | CYP3A4を介する本剤の代謝が阻害される。 |
| CYP3A誘導剤 リファンピシン等[16.7.3参照] |
本剤の血中濃度が低下し、効果が減弱するおそれがある。 | CYP3A4を介する本剤の代謝が促進される。 |
| P-糖蛋白阻害剤 シクロスポリン等[16.7.2参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。また、血液脳関門への影響により、本剤の脳内濃度が上昇するおそれがある。 | P-糖蛋白を介する本剤の輸送が阻害される。 |
有効性 ◆治療因子別の排便状況の改善割合(サブグループ解析)
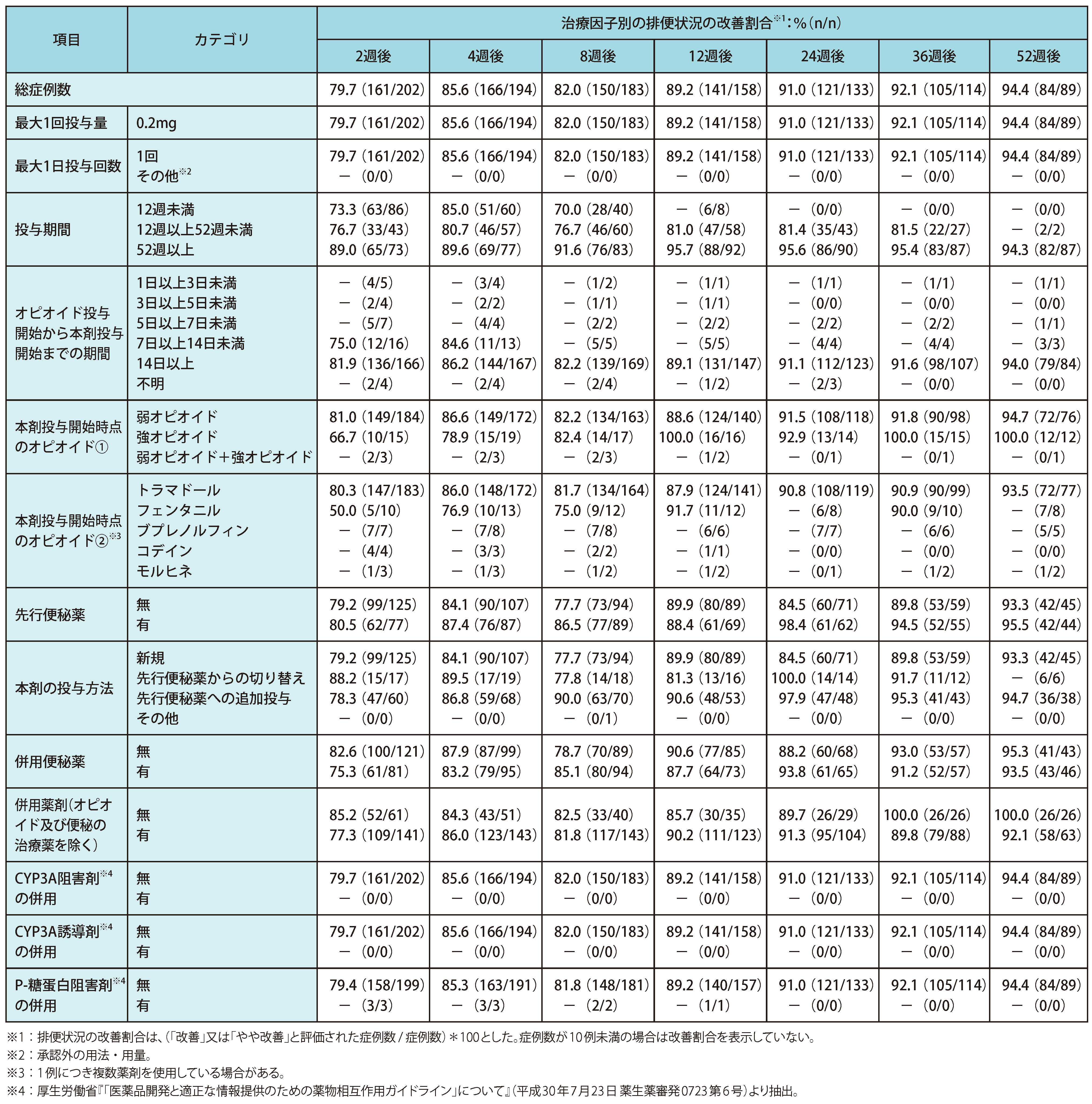
納谷憲幸,他.新薬と臨牀.2023;72:228-9.より作表
納谷憲幸、橋本佐代及び木屋昭憲は塩野義製薬株式会社の社員であり、石井清悟及び本田圭一はシオノギファーマコビジランスセンター株式会社の社員である。
本調査の実施及び本論文にかかわる費用は塩野義製薬株式会社が負担した。
【スインプロイク錠の相互作用(併用注意)】
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| CYP3A阻害剤 イトラコナゾール、フルコナゾール等 [16.7.4、16.7.5参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。 | CYP3A4を介する本剤の代謝が阻害される。 |
| CYP3A誘導剤 リファンピシン等[16.7.3参照] |
本剤の血中濃度が低下し、効果が減弱するおそれがある。 | CYP3A4を介する本剤の代謝が促進される。 |
| P-糖蛋白阻害剤 シクロスポリン等[16.7.2参照] |
本剤の血中濃度が上昇し、副作用が発現するおそれがある。また、血液脳関門への影響により、本剤の脳内濃度が上昇するおそれがある。 | P-糖蛋白を介する本剤の輸送が阻害される。 |

