ゾコーバ錠の臨床成績
国際共同第Ⅱ/Ⅲ相試験[T1221試験]第Ⅲ相パート(SCORPIO-SR試験)
「禁忌を含む注意事項等情報」等につきましては電子添文情報をご参照ください。
本剤は一部、承認外の用法・用量を含む臨床成績に基づいて承認されました。そのため、一部、承認外の用法・用量を含む試験成績を紹介しています。
社内資料:エンシトレルビルのSARS-CoV-2感染者対象第Ⅱ/Ⅲ相試験(Phase 3 Part)[承認時評価資料]
Yotsuyanagi H, et al. JAMA Netw Open. 2024 ; 7(2) : e2354991.
利益相反:本試験は塩野義製薬の支援により行われた。著者に塩野義製薬の社員を含む。
試験概要
- 目的
-
軽症/中等症のSARS-CoV-2感染者を対象に臨床症状改善効果を検証する
- 対象
-
12歳以上70歳未満の軽症/中等症のSARS-CoV-2感染者1,821例
- 評価
-
試験期間は28日間とし、21日間の有効性及び28日間の安全性を評価した
- 試験デザイン
-
多施設共同、ランダム化、二重盲検、プラセボ対照試験(日本、ベトナム、韓国の92施設で実施)
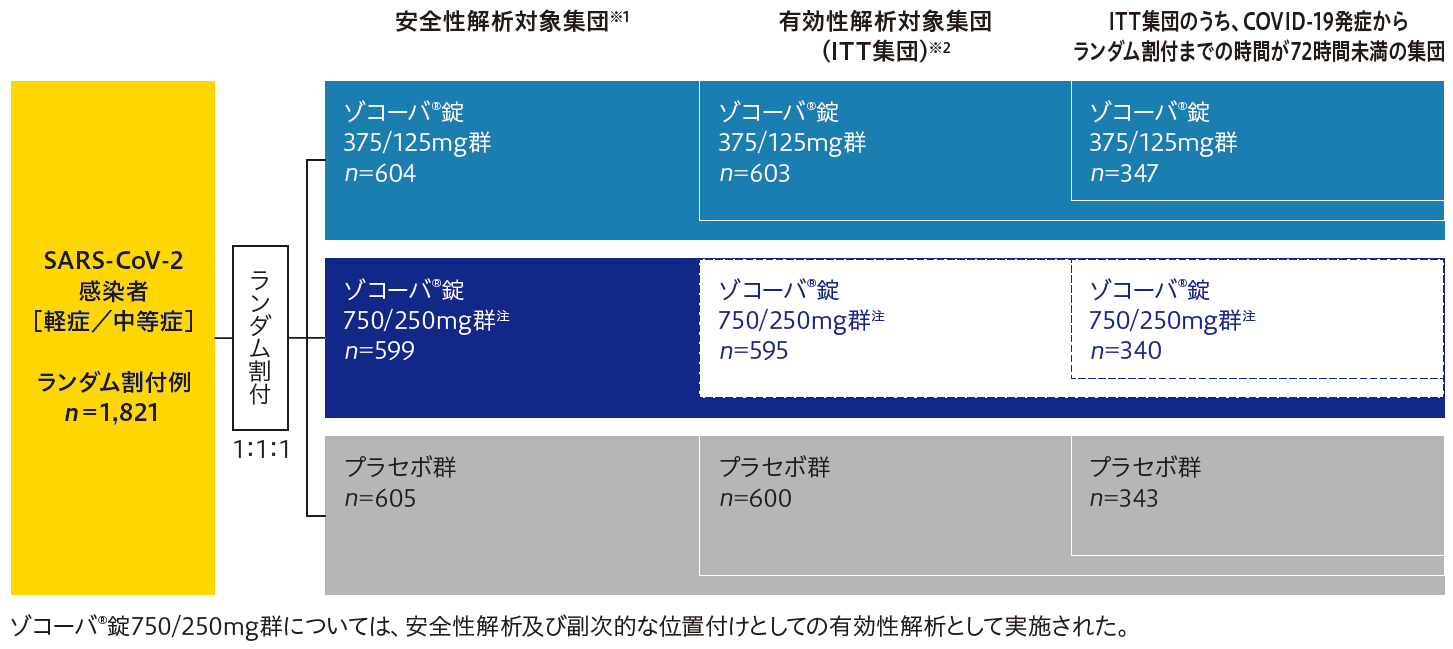
- ※1治験薬を少なくとも1回投与された被験者からなる集団。
- ※2intention-to-treat(ITT)集団。COVID-19発症からランダム割付までの時間が120時間以内で、かつ鼻咽頭ぬぐい液検体に基づくRTPCR の結果でSARS-CoV-2の感染が確認された被験者からなる集団。
- 投与方法
-
1日1回5日間、以下の用量を経口投与した。
● ゾコーバ錠375/125mg群:1日目に125mg錠×3錠及びプラセボ×3錠、2日目から5日目に125mg錠×1錠及びプラセボ×1錠を投与
● ゾコーバ錠750/250mg群注:1日目に250mg錠×3錠及びプラセボ×3錠、2日目から5日目に250mg錠×1錠及びプラセボ×1錠を投与
● プラセボ群:1日目にプラセボ×3錠及びプラセボ×3錠、2日目から5日目にプラセボ×1錠及びプラセボ×1錠を投与
注:承認外用法・用量
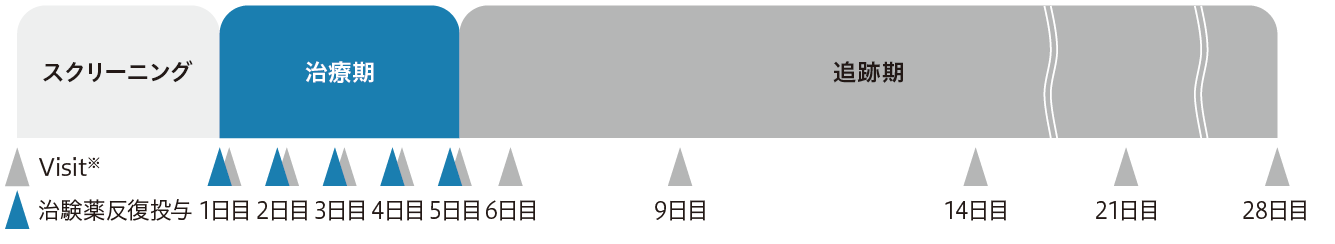
- ※3日目、5日目のVisitの実施は任意とした
6. 用法・用量
通常、12歳以上の小児及び成人にはエンシトレルビルとして1日目は375mgを、2日目から5日目は125mgを1日1回経口投与する。
- 選択基準
-
1. 12歳以上18歳未満かつ体重40kg以上又は18歳以上70歳未満
2. SARS-CoV-2陽性(ランダム化前120時間以内に採取された検体を用いたPCR検査等により確認)
3. SARS-CoV-2による感染症の症状(14症状※1のうち1つ以上)発現がランダム化前120時間以内
4. ランダム化時点において、SARS-CoV-2による感染症の症状(12症状)※2のうち、中等度(スコア2)※3以上の症状が1つ以上認められる。ただし、SARS-CoV-2による感染症の発症前から存在した症状である場合は、SARS-CoV-2による感染症により悪化したと被験者が判断した症状に限る
5. 治験薬投与開始~投与終了後少なくとも10日間避妊が可能な者
6. (女性のみ)妊婦ではなく、妊娠している可能性もない者
- 除外基準
-
1. SpO2が93%以下(室内気)
2. 酸素投与を要する
3. 人工呼吸器を要する
4. 中等度以上(CTCAE第5.0版Grade 2以上)の肝疾患の現病歴又は慢性病歴を有する
5. 中等度以上(CTCAE第5.0版Grade 2以上)の腎疾患の現病歴又は慢性病歴を有する
- 評価項目
-
主要評価項目:COVID-19の5症状※4が快復するまでの時間※5
主要な副次評価項目:
4日目におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量(A)
SARS-CoV-2のウイルス力価陰性が最初に確認されるまでの時間(B)
その他の副次評価項目:
COVID-19の12症状※2が快復するまでの時間
COVID-19の14症状※1が快復するまでの時間
各時点におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量(21日目まで)
各時点におけるSARS-CoV-2のウイルス力価のベースラインからの変化量(21日目まで) など
安全性評価項目:有害事象及び副作用の発現状況
- 解析計画(有効性、一部抜粋)
-
・ 主要評価項目に対する主解析は検証的な解析項目として、ITT集団※6のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団を対象に、SARS-CoV-2による感染症に対するワクチン接種の有無を層とするPeto-Prenticeの層別一般化Wilcoxon検定を用いて両側有意水準0.05でCOVID‑19の5症状が快復するまでの時間についてゾコーバ錠375/125mg群とプラセボ群の間で比較を行った。また、主要な副次解析として、ITT集団を対象に主解析と同様の解析を行った。このとき、SARS-CoV-2による感染症に対するワクチン接種の有無に加えて、COVID-19発症からランダム割付までの時間(72時間未満、72時間以上)も層に含めた。
・ 主要な副次評価項目である4日目におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量に対する主解析として、ITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団を対象に、SARS-CoV-2のウイルスRNA量のベースラインからの変化量を応答、SARS-CoV-2による感染症に対するワクチン接種の有無、及びベースライン時のSARS-CoV-2のウイルスRNA量を共変量とする共分散分析を適用し、両側有意水準0.05でゾコーバ錠375/125mg群とプラセボ群の間で比較を行った。また、主要な副次解析として、ITT集団を対象に同様の解析を行った。
このとき、SARS-CoV-2による感染症に対するワクチン接種の有無、及びベースライン時のSARSCoV-2のウイルスRNA量に加えて、COVID-19発症からランダム割付までの時間(72時間未満、72時間以上)も共変量に含めた。
・ 主要な副次評価項目であるSARS-CoV-2のウイルス力価陰性が最初に確認されるまでの時間に対する主解析として、mITT集団※7のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団を対象に、SARS-CoV-2による感染症に対するワクチン接種の有無を層とする層別log-rank検定を用いて、両側有意水準0.05でSARS-CoV-2のウイルス力価陰性が最初に確認されるまでの時間についてゾコーバ錠375/125mg群とプラセボ群の間で比較を行った。主要な副次解析として、mITT集団を対象に同様の解析を実施した。このとき、SARS-CoV-2による感染症に対するワクチン接種の有無に加えて、COVID-19発症からランダム割付までの時間(72時間未満、72時間以上)も層に含めた。
・ これらの評価項目について、ゾコーバ錠375/125mg群とプラセボ群との比較に対して固定順序法に基づく第1種の過誤率の制御を行った。多重性調整を行う比較は以下の手順とした。
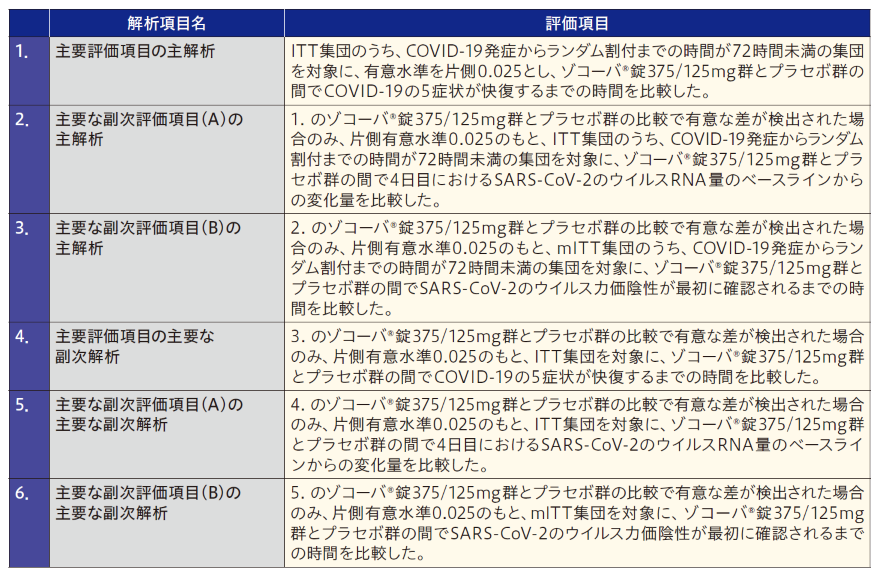
- 解析計画
-
固定順序法の解析方法に基づき、主要評価項目の主要な副次解析(4. COVID-19の5症状が快復するまでの時間)で統計学的有意差が認められなかったため、検定の手順を終了した。それ以降のデータ(4. COVID-19の5症状が快復するまでの時間、5. 4日目におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量、6. SARS-CoV-2のウイルス力価陰性が最初に確認されるまでの時間)については当資材に含めていない。
・その他の副次評価項目であるCOVID-19の12症状、及び14症状が快復するまでの時間と各時点におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量、各時点におけるSARS-CoV-2のウイルス力価のベースラインからの変化量の主解析としてITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団を対象に比較を行った。
・ その他の副次評価項目であるCOVID-19の12症状、及び14症状が快復するまでの時間に対して、COVID-19の5症状が快復するまでの時間と同様の解析を行った。COVID-19の14症状の快復は、主要評価項目に記載した快復の定義に加え、治験薬投与開始時点から味覚異常、及び嗅覚異常が下記の通りに快復した時点を指し、その状態が少なくとも24時間持続したとき、快復と判断した。
・ COVID-19発症前から存在した既存症状で、ベースライン(投与前検査)時点で悪化していると被験者が判断した症状については、ベースライン時点の重症度から改善又は維持する必要がある。
・ COVID-19発症前から存在した既存症状で、ベースライン(投与前検査)時点で悪化していないと被験者が判断した症状については、ベースライン時点の重症度を維持又は改善する必要がある。
・上記以外の症状、すなわちCOVID-19発症前には存在しておらず、ベースライン(投与前検査)時点あるいはそれ以降に発現した症状については、症状が「通常通り」になる必要がある。
- ※1①倦怠感又は疲労感、②筋肉痛又は体の痛み、③頭痛、④悪寒又は発汗、⑤熱っぽさ又は発熱、⑥鼻水又は鼻づまり、⑦喉の痛み、⑧咳、⑨息切れ(呼吸困難)、⑩吐き気、⑪ 嘔吐、⑫下痢、⑬味覚異常、⑭嗅覚異常。14症状のうち①~⑫の12症状は、被験者日誌でそれぞれ4段階(0:なし、1:軽度、2:中等度、3:重度)で、⑬、⑭は、それぞれ3 段階(0:通常通り、1:通常に比べて感じない、2:全く感じない)で評価した。
- ※2①倦怠感又は疲労感、②筋肉痛又は体の痛み、③頭痛、④悪寒又は発汗、⑤熱っぽさ又は発熱、⑥鼻水又は鼻づまり、⑦喉の痛み、⑧咳、⑨息切れ(呼吸困難)、⑩吐き気、⑪ 嘔吐、⑫下痢。12症状は、被験者日誌でそれぞれ4段階( 0:なし、1:軽度、2:中等度、3:重度)で評価した。
- ※3症状のスコアを被験者本人が4段階(0:なし、1:軽度、2:中等度、3:重度)で評価した。
- ※4①倦怠感又は疲労感、②熱っぽさ又は発熱、③鼻水又は鼻づまり、④喉の痛み、⑤咳。5症状は、被験者日誌でそれぞれ4段階(0:なし、1:軽度、2:中等度、3:重度)で評価した。
- ※5治験薬投与開始時点からCOVID-19症状のうち評価対象の症状すべてが下記の定義を満たす状態に至った時点を指し、その状態が少なくとも24時間持続したとき、当該被験者のCOVID-19症状は快復したと判断した。
・ SARS-CoV-2による感染症の発症前から存在した既存症状で、ベースライン(投与前検査)時点で悪化していると被験者が判断した症状については、ベースライン時の重症度が重度のものは中等度以下、中等度のものは軽度以下、軽度のものは軽度以下へ重症度が改善又は維持した状態となること。
・ SARS-CoV-2による感染症の発症前から存在した既存症状で、ベースライン(投与前検査)時点で悪化していないと被験者が判断した症状については、ベースライン時の重症度が重度のものは重度以下、中等度のものは中等度以下、軽度のものは軽度以下へ重症度が維持又は改善した状態となること。
・上記以外の症状[SARS-CoV-2による感染症の発症前には存在しておらず、ベースライン(投与前検査)時点以降に発現した症状]については、なしの状態となること。 - ※6intention-to-treat(ITT)集団。COVID-19発症からランダム割付までの時間が120時間以内で、かつ鼻咽頭ぬぐい液検体に基づくRT-PCRの結果でSARS-CoV-2の感染 が確認された被験者からなる集団。
- ※7modified intention-to-treat(mITT)集団。ITT集団のうち、ベースラインでのウイルス力価が検出された被験者からなる集団。
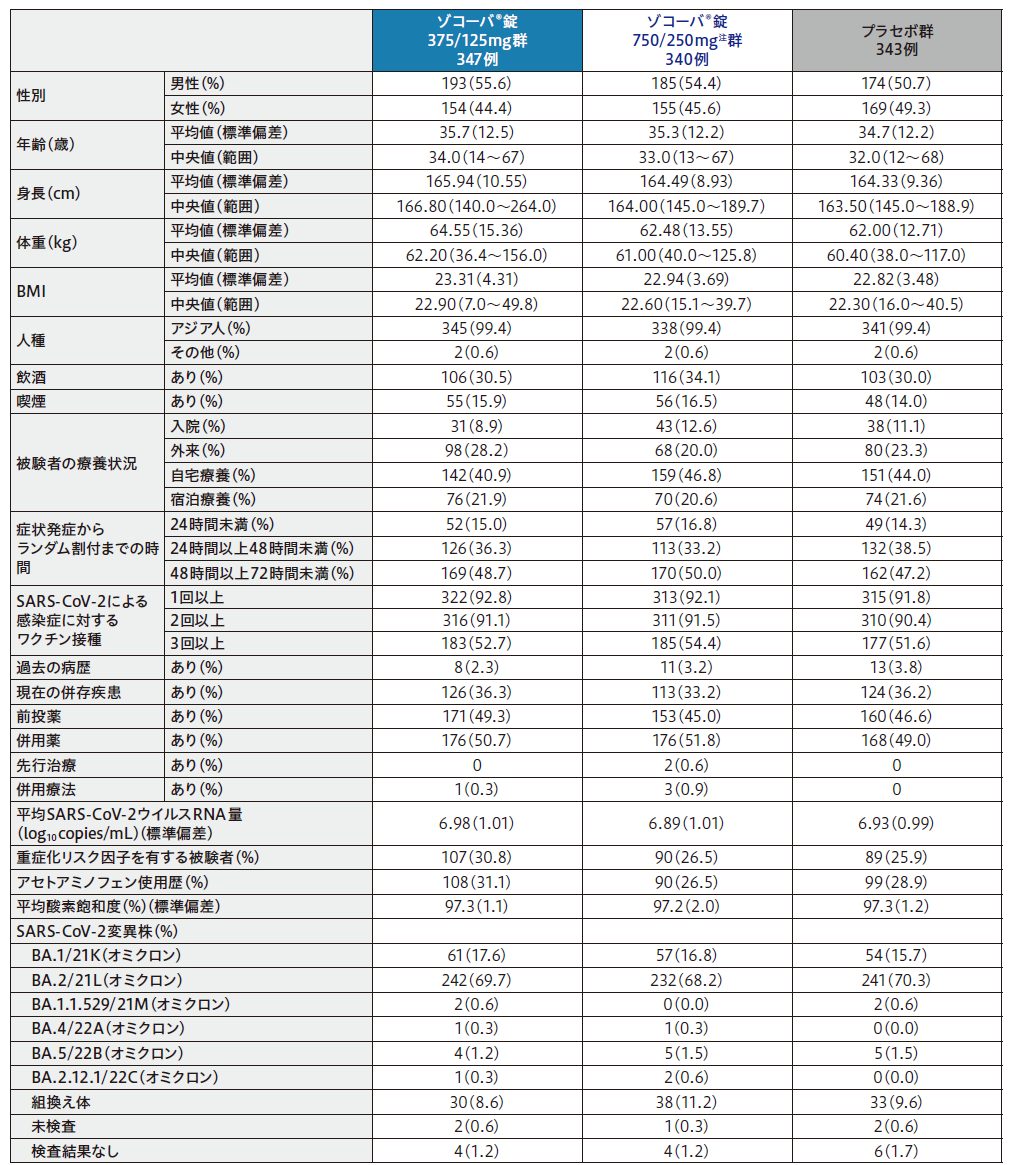
患者背景
(ITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団)
主要評価項目: COVID-19の5症状が快復するまでの時間
(主解析:ITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団)
COVID-19の5症状※1が快復するまでの時間※2は、プラセボ群と比較してゾコーバ錠375/125mg群で統計学的に有意に短いことが検証された(p=0.0407) (検証的な解析結果)。
主要評価項目:COVID-19の5症状※1が快復するまでの時間※2のKaplan-Meier曲線
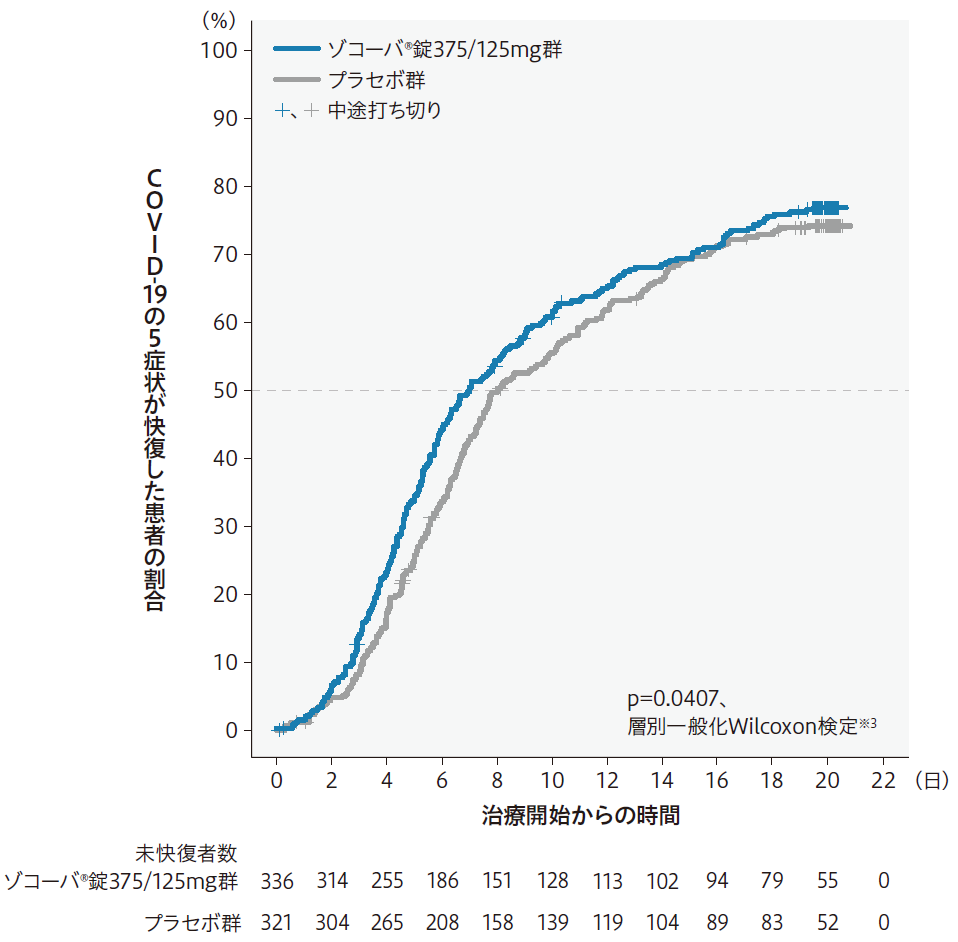
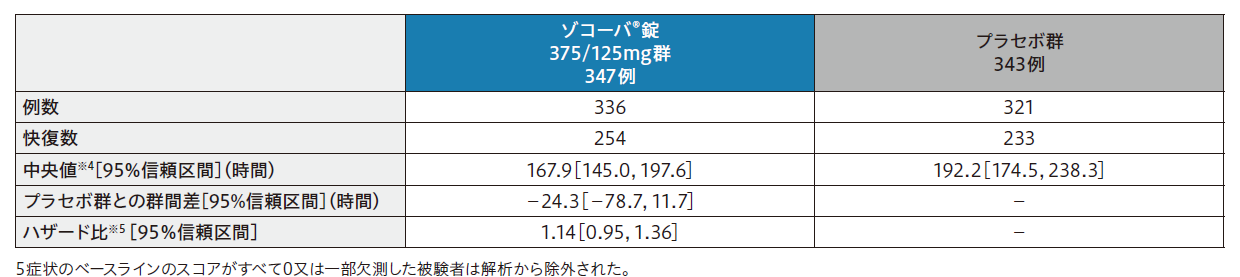
- ※1①倦怠感又は疲労感、②熱っぽさ又は発熱、③鼻水又は鼻づまり、④喉の痛み、⑤咳。5症状は、被験者日誌でそれぞれ4段階(0:なし、1:軽度、2:中等度、3:重度)で評価した。
- ※2治験薬投与開始時点からCOVID-19症状のうち評価対象の症状すべてが下記の定義を満たす状態に至った時点を指し、その状態が少なくとも24時間持続したとき、当該被験者のCOVID-19症状は快復したと判断した。
・SARS-CoV-2による感染症の発症前から存在した既存症状で、ベースライン(投与前検査)時点で悪化していると被験者が判断した症状については、ベースライン時の重症度が重度のものは中等度以下、中等度のものは軽度以下、軽度のものは軽度以下へ重症度が改善又は維持した状態となること。
・SARS-CoV-2による感染症の発症前から存在した既存症状で、ベースライン(投与前検査)時点で悪化していないと被験者が判断した症状については、ベースライン時の重症度が重度のものは重度以下、中等度のものは中等度以下、軽度のものは軽度以下へ重症度が維持又は改善した状態となること。
・上記以外の症状[SARS-CoV-2による感染症の発症前には存在しておらず、ベースライン(投与前検査)時点以降に発現した症状]については、なしの状態となること。 - ※3有意水準両側0.05、SARS-CoV-2による感染症に対するワクチン接種の有無を層とするPeto-Prenticeの層別一般化Wilcoxon検定。
- ※4COVID-19の5症状が快復した被験者の割合が50%となるまでの時間。
- ※5SARS-CoV-2による感染症に対するワクチン接種の有無を層とした層別Coxハザードモデル。
注: ゾコーバ錠750/250mg群は本邦未承認用法・用量であり、有効性の結果は掲載していません。
主要な副次評価項目: 4日目におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量
(ITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団)
4日目におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量の調整済み推定値は、ゾコーバ錠375/125mg群-2.48log10copies/mL、プラセボ群-1.01log10copies/mLであり、その差は-1.47log10copies/mLで、統計学的に有意に減少した(p<0.0001)。
4日目におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量
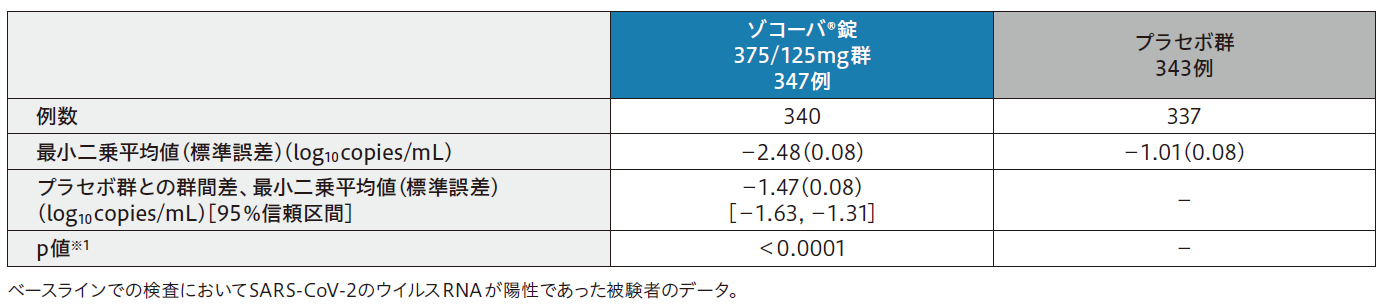
- ※1ベースラインでのSARS-CoV-2のウイルスRNA量、及びSARS-CoV-2による感染症に対するワクチンの接種の有無を共変量とする共分散分析。
注:ゾコーバ錠750/250mg群は本邦未承認用法・用量であり、有効性の結果は掲載していません。
その他の副次評価項目: 各時点におけるSARS-CoV-2のウイルスRNA量のベースラインからの変化量
(21日目まで)
(ITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団)
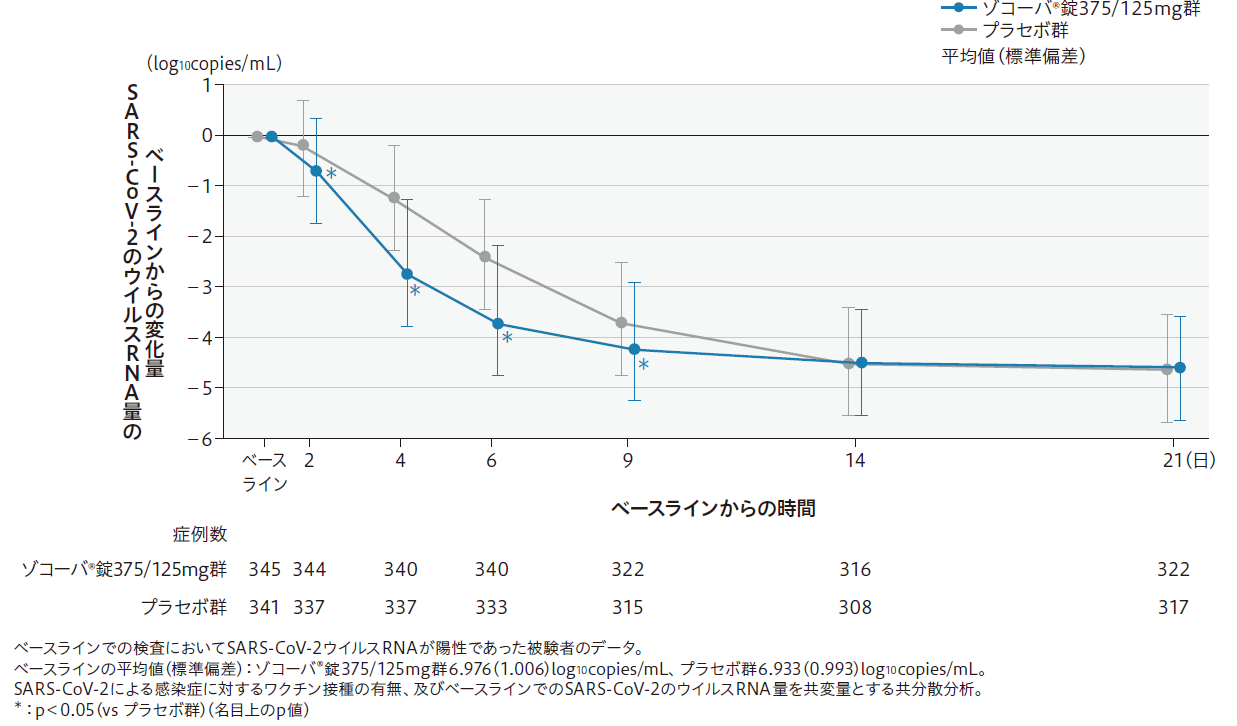
注:ゾコーバ錠750/250mg群は本邦未承認用法・用量であり、有効性の結果は掲載していません。
主要な副次評価項目: SARS-CoV-2のウイルス力価陰性が最初に確認されるまでの時間
(mITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団)
SARS-CoV-2のウイルス力価陰性が最初に確認されるまでの時間は、プラセボ群と比較してゾコーバ錠375/125mg群で有意に短かった(p<0.001)。
SARS-CoV-2のウイルス力価陰性が最初に確認されるまでの時間のKaplan-Meier曲線
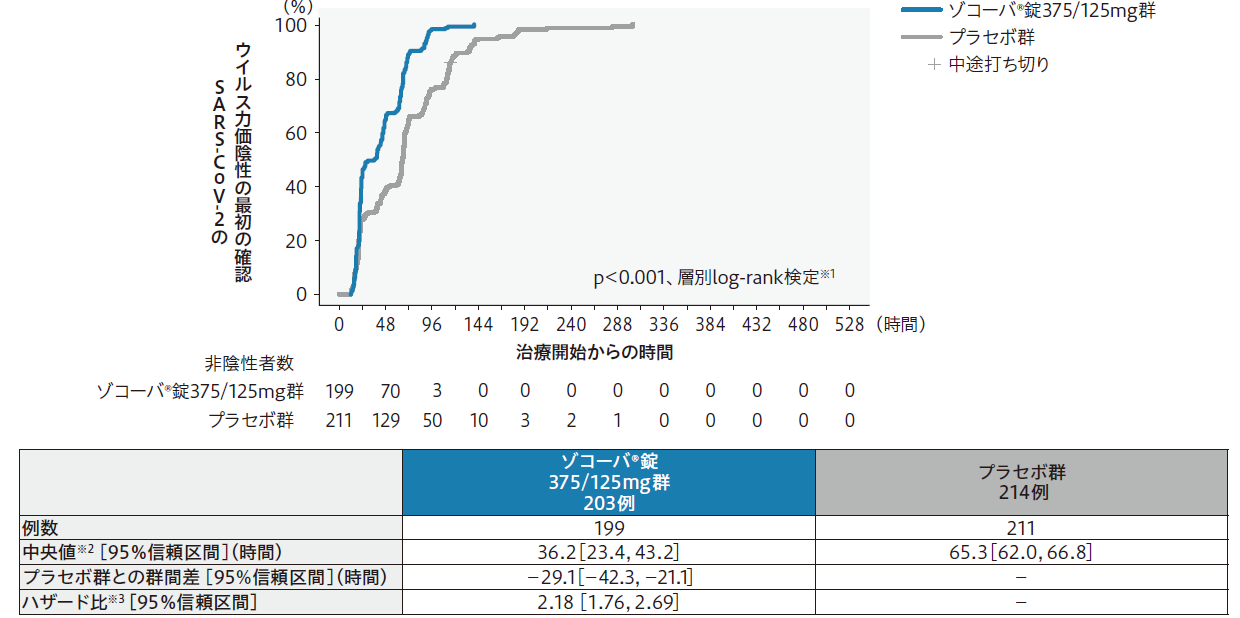
- ※1有意水準片側0.025、SARS-CoV-2による感染症に対するワクチン接種の有無を層とする層別log-rank検定。
- ※2SARS-CoV-2のウイルス力価陰性が最初に確認された被験者の割合が50%となるまでの時間。
- ※3SARS-CoV-2による感染症に対するワクチン接種の有無を層とした層別Coxハザードモデル。
注:ゾコーバ錠750/250mg群は本邦未承認用法・用量であり、有効性の結果は掲載していません。
その他の副次評価項目: 各時点におけるSARS-CoV-2のウイルス力価のベースラインからの変化量 (21日目まで)
(mITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団)
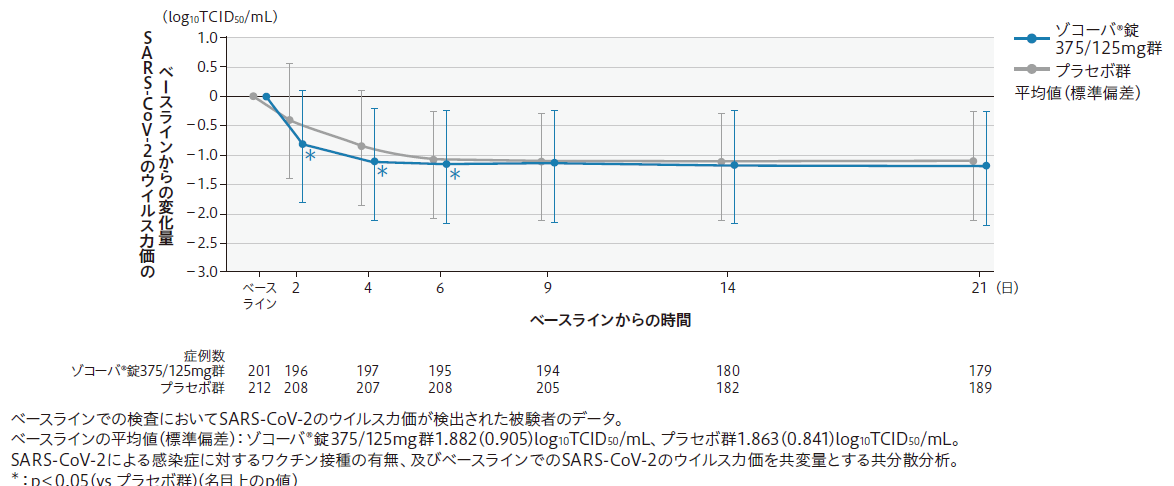
注:ゾコーバ錠750/250mg群は本邦未承認用法・用量であり、有効性の結果は掲載していません。
その他の副次評価項目: COVID-19の12症状が快復するまでの時間、及びCOVID-19の14症状が快復するまでの時間
(ITT集団のうち、COVID-19発症からランダム割付までの時間が72時間未満の集団)
COVID-19の12症状※1が快復するまでの時間は、プラセボ群と比較してゾコーバ錠375/125mg群で統計学的に有意な差は認められなかった。
COVID-19の14症状※2が快復するまでの時間は、プラセボ群と比較してゾコーバ錠375/125mg群で統計学的に有意に短かった(p=0.0304、名目上のp値)。
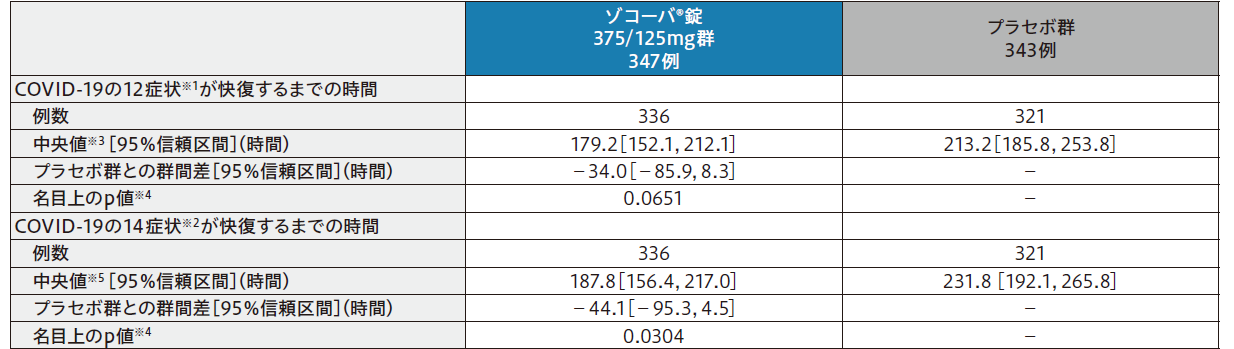
- ※1①倦怠感又は疲労感、②筋肉痛又は体の痛み、③頭痛、④悪寒又は発汗、⑤熱っぽさ又は発熱、⑥鼻水又は鼻づまり、⑦喉の痛み、⑧咳、⑨息切れ(呼吸困難)、⑩吐き気、⑪嘔 吐、⑫下痢。12症状は、被験者日誌でそれぞれ4段階(0:なし、1:軽度、2:中等度、3:重度)で評価した。
- ※2①倦怠感又は疲労感、②筋肉痛又は体の痛み、③頭痛、④悪寒又は発汗、⑤熱っぽさ又は発熱、⑥鼻水又は鼻づまり、⑦喉の痛み、⑧咳、⑨息切れ(呼吸困難)、⑩吐き気、 ⑪嘔吐、⑫下痢、⑬味覚異常、⑭嗅覚異常。14症状のうち①~⑫の12症状は、被験者日誌でそれぞれ4段階(0:なし、1:軽度、2:中等度、3:重度)で、⑬、⑭は、それぞ れ3段階(0:通常通り、1:通常に比べて感じない、2:全く感じない)で評価した。
- ※3COVID-19の12症状が快復した被験者の割合が50%となるまでの時間。
- ※4SARS-CoV-2による感染症に対するワクチン接種の有無を層とするPeto-Prenticeの層別一般化Wilcoxon検定。
- ※5COVID-19の14症状が快復した被験者の割合が50%となるまでの時間。
注:ゾコーバ錠750/250mg群は本邦未承認用法・用量であり、有効性の結果は掲載していません。
安全性
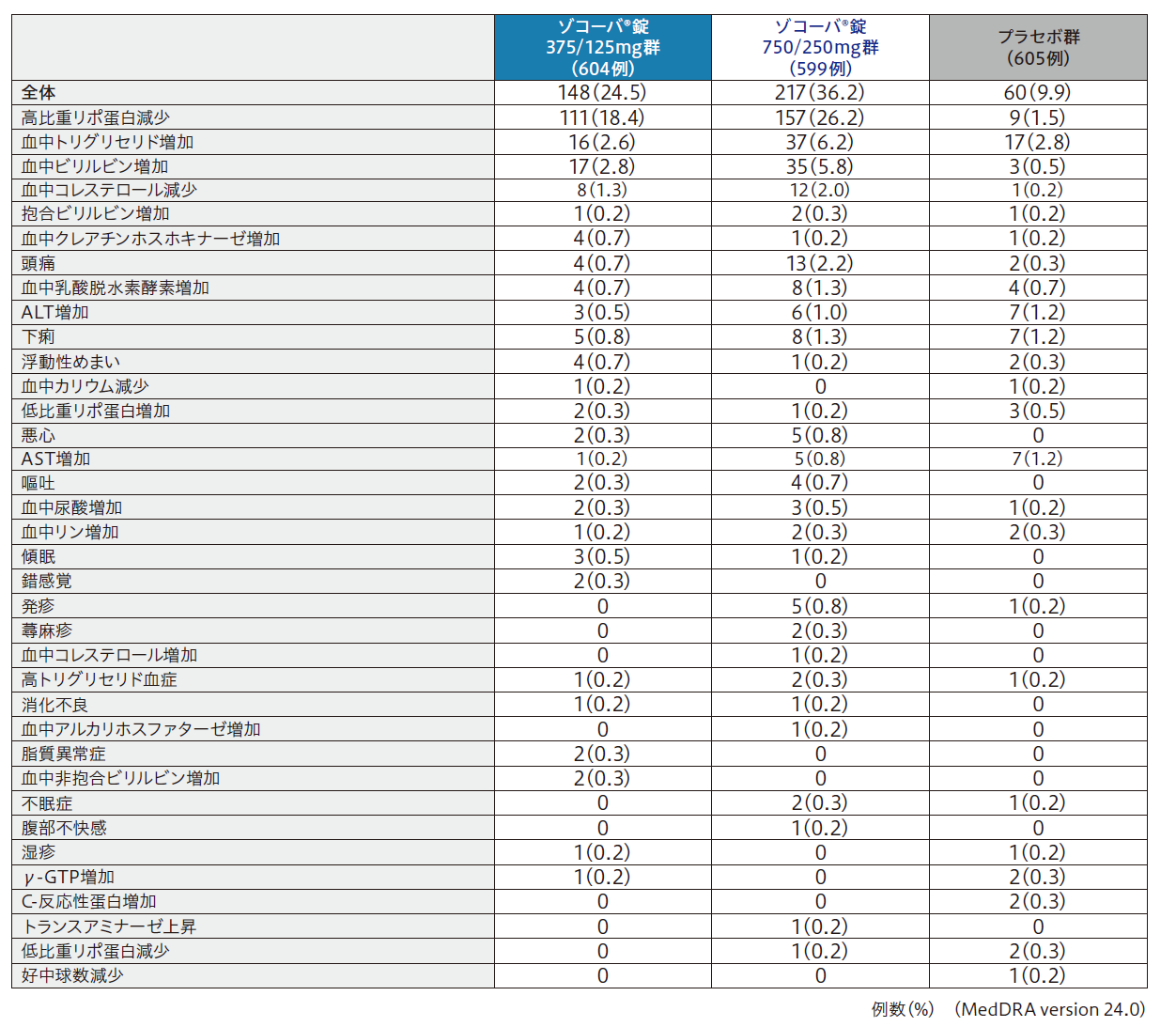
副作用の発現率はゾコーバ錠375/125mg群24.5%(148/604例)、ゾコーバ錠750/250mg群36.2%(217/599例)、プラセボ群9.9%(60/605例)であった。
2%以上に報告された副作用は、ゾコーバ錠375/125mg群では高比重リポ蛋白減少18.4%(111/604例)、血中ビリルビン増加2.8%(17/604例)、血中トリグリセリド増加2.6%(16/604例)、ゾコーバ錠750/250mg群では高比重リポ蛋白減少26.2%(157/599例)、血中トリグリセリド増加6. 2%(37/599例)、血中ビリルビン増加5. 8%(35/599例)、頭痛2. 2%(13/599例)、血中コレステロール減少2.0%(12/599例)であった。プラセボ群では血中トリグリセリド増加2.8%(17/605例)であった。
本試験においていずれの群でも死亡は認められなかった。また、重篤な有害事象としてゾコーバ錠375/125mg群で重度月経出血、プラセボ群で急性胆嚢炎がそれぞれ1例に認められたが、いずれも治験薬との因果関係なしと判断された。
投与中止に至った副作用は、ゾコーバ錠375/125mg群で2例2件(湿疹及び嘔吐)、ゾコーバ錠750/250mg群で2例2件(軽度及び中等度の発疹)、プラセボ群で1例2件(筋力低下及び感覚鈍麻)に認められた。
副作用の発現状況
6. 用法・用量
通常、12歳以上の小児及び成人にはエンシトレルビルとして1日目は375mgを、2日目から5日目は125mgを1日1回経口投与する。
その他のゾコーバ関連情報
-
会員限定
COVID-19治療に関する情報
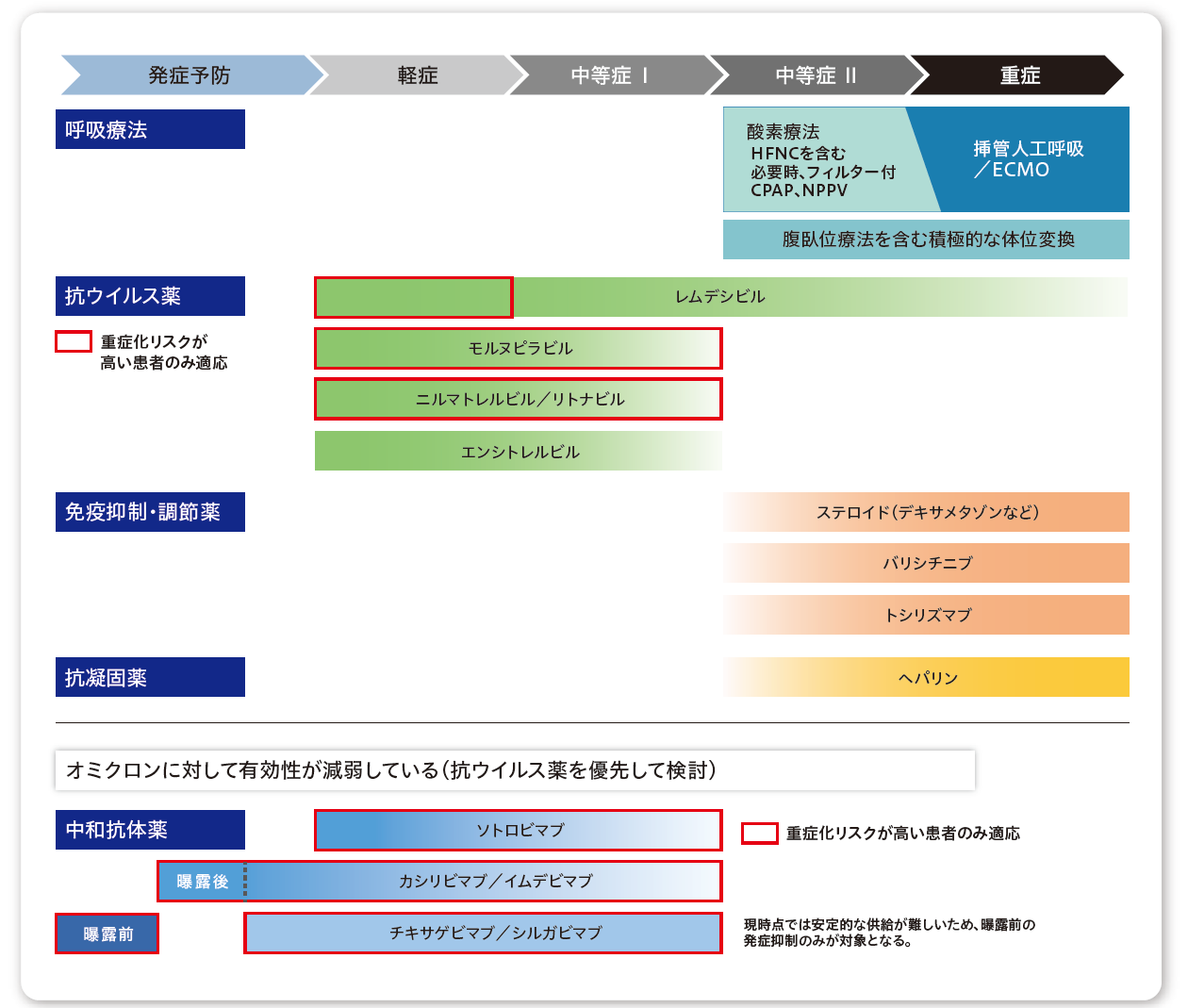
COVID-19における重症度別マネジメントや重症度分類、重症化リスク等について厚生労働省「新型コロナウイルス感染症(COVID-19)診療の手引き・第10.1版」や米国CDCからの情報をご紹介しております。
-
市販後の安全性情報
令和4年11月22日に緊急承認医薬品として承認を取得して以降、令和4年11月24日から令和6年3月5日までに報告された症例情報(推定1,063,688人)及び副作用等を集計しております。

-
一般使用成績調査<最終集計報告>
ゾコーバ錠の使用実態下における本剤の安全性及び有効性に関する情報を収集することを目的として、2022年11月から2024年2月まで実施した一般使用成績調査の最終集計報告(収集症例4,125例)です。
