フェトロージャの概要
薬剤耐性菌の脅威
薬剤耐性菌が世界的に増加する一方、新規抗菌薬の開発は減少傾向にあり、国際社会でも大きな課題となっています。
CDC(Centers for Disease Control and Prevention:米国疾病管理・予防センター)による報告では、カルバペネム耐性腸内細菌目細菌(CRE)感染症の割合が10年間で4倍に増加し1)、米国では年間9,000人が感染し、600人が死亡していると注意喚起しています(2013年時点)2)。
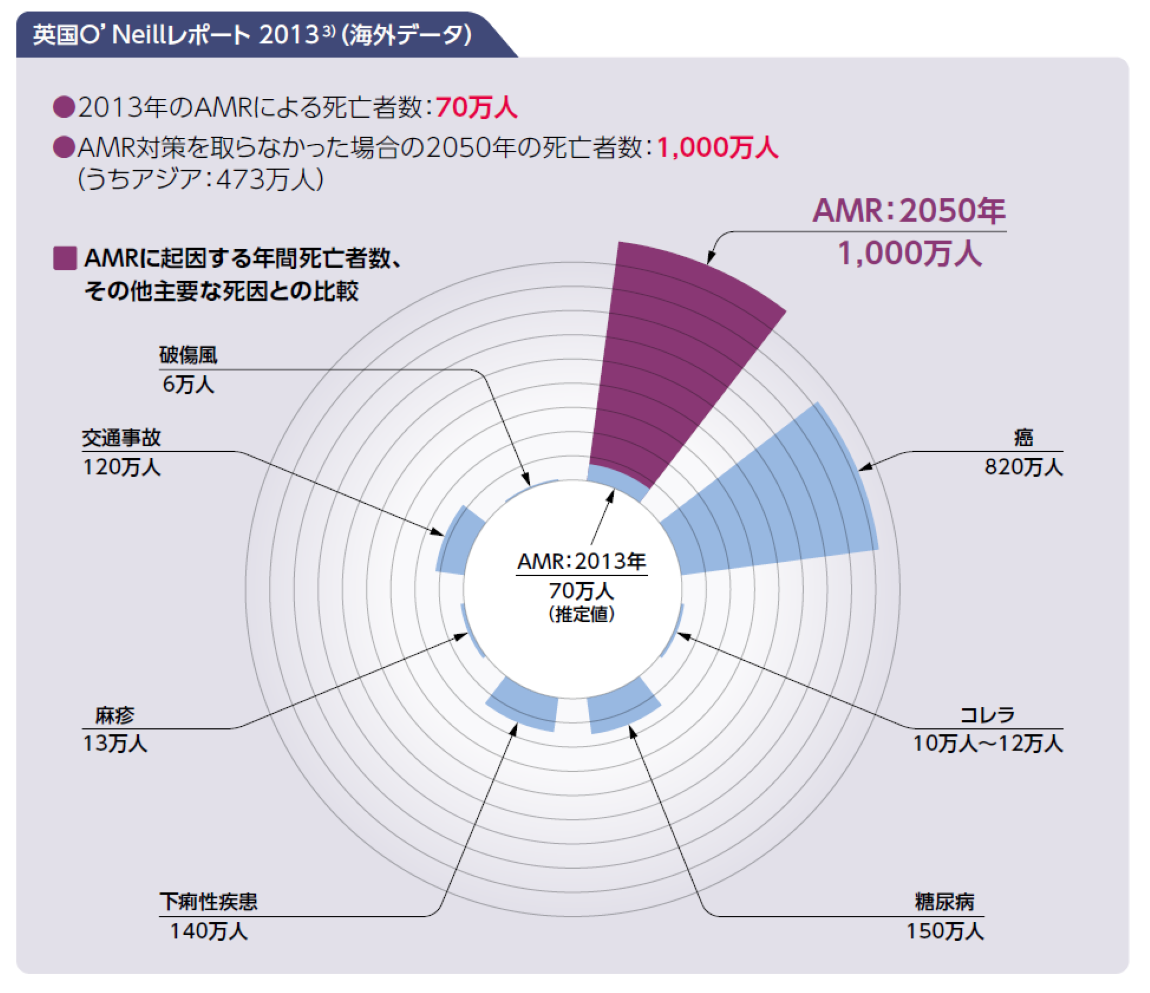
また、英国のO’Neillレポートでは、AMR(Antimicrobial Resistance:薬剤耐性)対策を取らなかった場合、 2050年には世界全体で年間1,000万人がAMRで死亡する、と推測しています(2013年時点)3)。
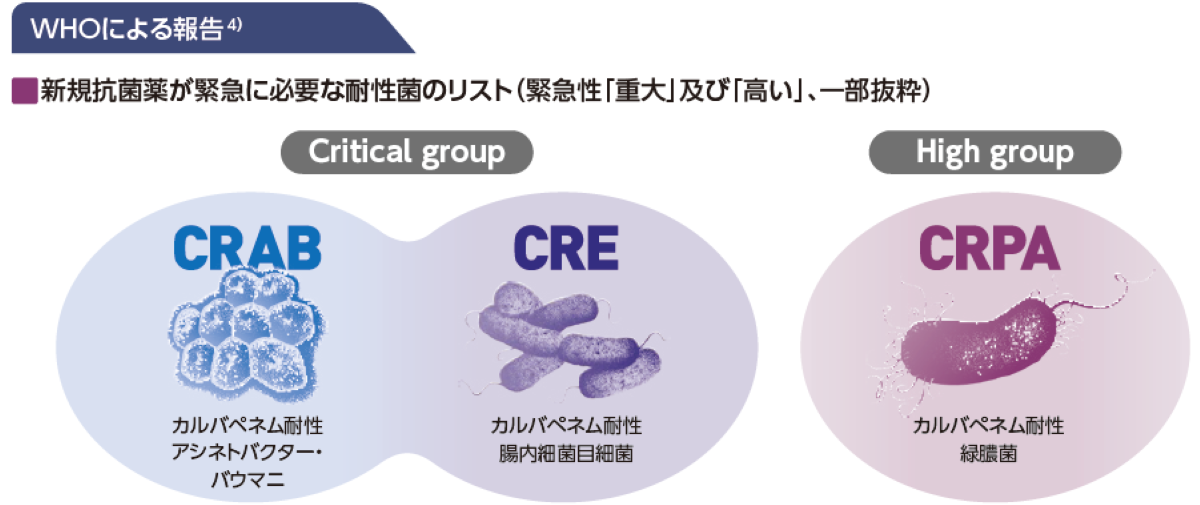
さらにWHOは、2024年に新規抗菌薬開発が必要な15種類の薬剤耐性菌リストを公表しました。緊急性が「重大」な菌種として、カルバペネム耐性アシネトバクター・バウマニ(CRAB)、第3世代セファロスポリン耐性腸内細菌目細菌(3GCRE)、カルバペネム耐性腸内細菌目細菌(CRE)を挙げ、緊急性が「高い」グループの一つにカルバペネム耐性緑膿菌(CRPA)を位置付け、 新たな抗微生物薬開発の必要性を訴えています4)。

フェトロージャの作用機序と耐性克服機序
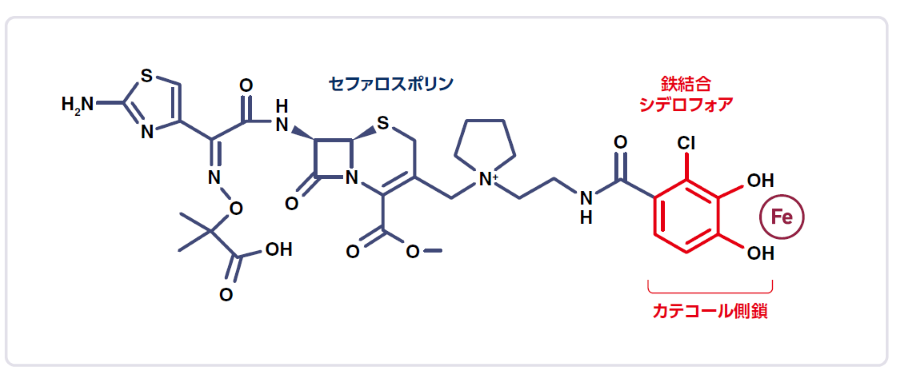
フェトロージャの構造式
フェトロージャは生体内の鉄と結合する構造をもつ、世界で唯一のセファロスポリン系抗生物質です。
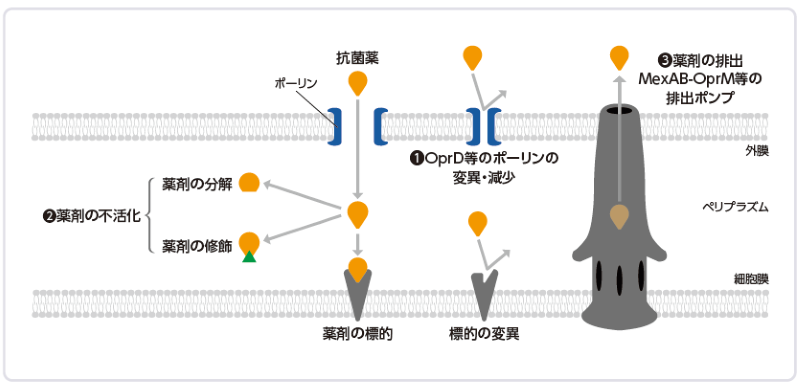
主な薬剤耐性機序
グラム陰性桿菌のカルバペネム系薬に対する耐性機序には、
❶外膜変化による外膜透過性低下
❷β-ラクタマーゼによる薬剤の不活化
❸多剤排出ポンプによる能動的な薬剤排出
等があります。
また、複数の耐性機序が併存することがあります。
日本環境感染学会 多剤耐性菌感染制御委員会:環境感染誌, 32, Suppl.Ⅲ, 2017, S1-S25
フェトロージャの作用機序と耐性克服機序
フェトロージャは細菌が自ら鉄を取り込む性質を利用した世界初の作用機序を有する薬剤です。
これにより、カルバペネム耐性菌の主要な耐性機序の1つである外膜透過性低下を回避します。
さらに、各種β-ラクタマーゼに対し高い安定性を有し、排出ポンプ高産生の影響を受けにくいという特徴を有します。
これらの機序によって既存のβ-ラクタム耐性を克服し、標的であるペニシリン結合タンパク質に結合することで細胞壁合成を阻害します。
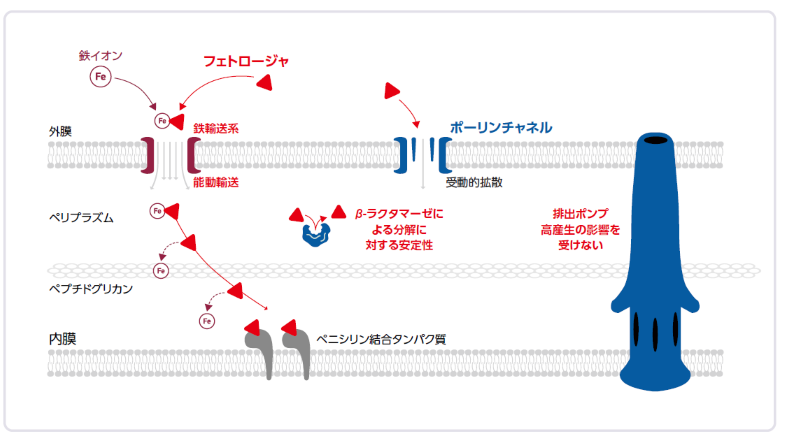
Zhanel, GG. et al.: Drugs, 2019, 79(3), 271より作図
著者に塩野義製薬株式会社より研究助成金を受領している者が含まれる。
CRE病原体サーベイランス
カルバペネマーゼの検出割合
国内で検出されるカルバペネマーゼは、メタロβ-ラクタマーゼが約97%を占めています。
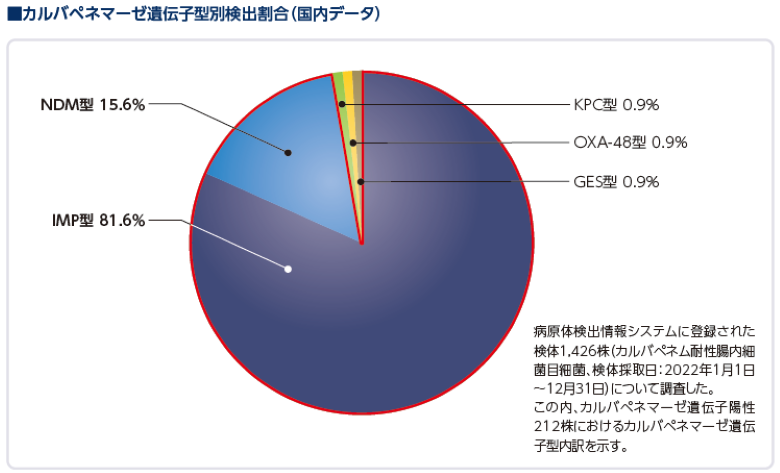
IASR, Vol. 45, 129-130, 2024年7月号より作図
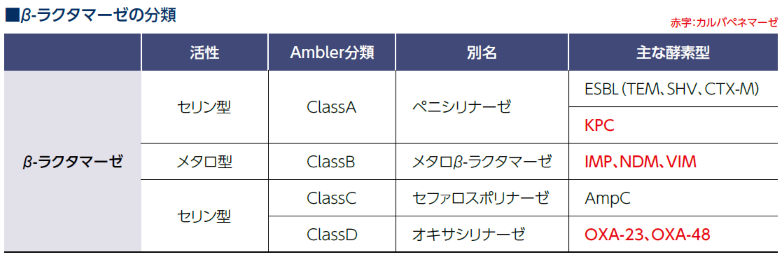
中村明子ほか:THE CHEMICAL TIMES, 2016, 1, 239, 10
石井良和:日本臨床微生物学雑誌, 2014, 24(3), 171より作表
ESBL : extended-spectrum β-lactamase、基質拡張型β-ラクタマーゼ
KPC : Klebsiella pneumoniae carbapenemase、クラスA カルバペネマーゼの一つ
IMP : imipenemase、クラスB カルバペネマーゼの一つ
NDM : New Delhi metallo-β-lactamase、クラスB カルバペネマーゼの一つ
VIM : Verona integron-encoded metallo-β-lactamase、クラスB カルバペネマーゼの一つ
AmpC: class C ampicillinase、クラスC β-ラクタマーゼの一つ
OXA : oxacillinase、クラスD カルバペネマーゼの一つ
GES : Guiana extended-spectrum β-lactamase、クラスA カルバペネマーゼの一つ
フェトロージャの構造上の特徴
フェトロージャの構造上の特徴
フェトロージャは β-ラクタマーゼへの安定性を高める3つの側鎖を修飾することで、メタロ型を含むすべての β-ラクタマーゼに安定です。
そのためカルバペネマーゼの中で日本で最も検出頻度の高いメタロ β-ラクタマーゼ産生菌に対して、単剤で有効性が期待できます(カルバペネム系抗菌薬に耐性を示す菌株に限る)。
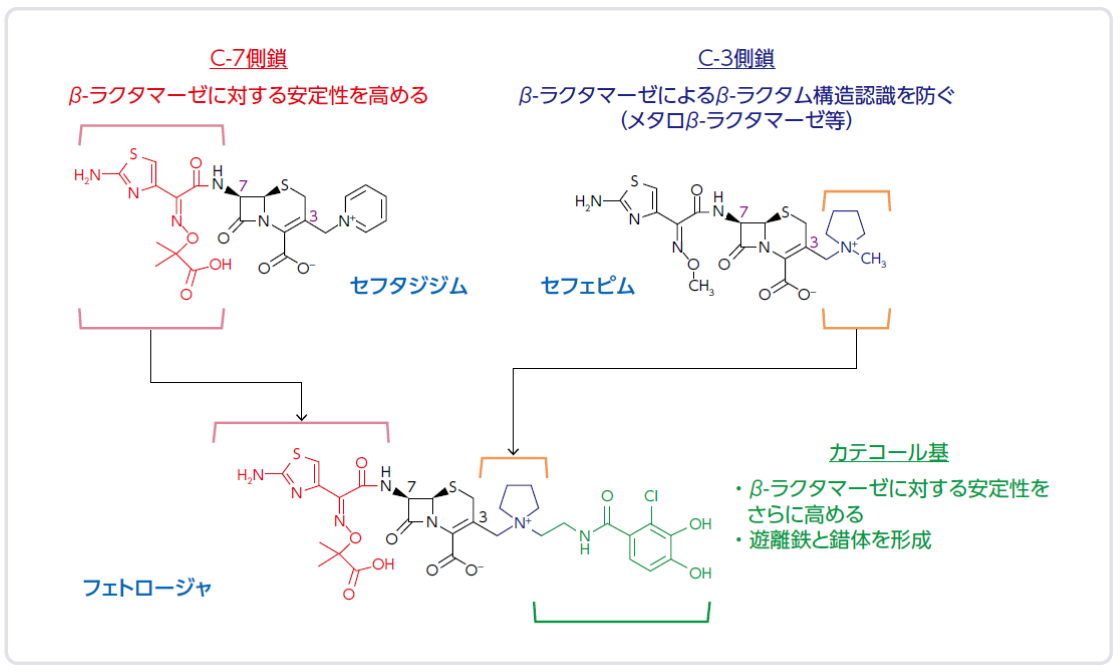
フェトロージャは、抗菌薬耐性グラム陰性菌に対する活性を高めるため、いくつかの特有の分子構造を有しています(上図)。
第三~第四世代のセファロスポリン系抗生物質であるセフタジジムやセフェピムは、クラスC β-ラクタマーゼの一つであるAmpCや基質拡張型β-ラクタマーゼ(ESBL)を含む様々なβ-ラクタマーゼに対する高い安定性により、グラム陰性菌に対して良好な活性を示します。
フェトロージャは、これらの抗生物質と同様の安定性を得るため、セフェピムと同様に3位にピロリジニウム基を、セフタジジムと同様に7位側鎖にカルボキシプロピルオキシイミノ基を有しています。さらにフェトロージャは、カルバペネマーゼに対するさらなる安定性獲得のため、3位側鎖にカテコール基を有しています。
Zhanel, GG. et al.: Drugs, 2019, 79(3), 271
著者に塩野義製薬株式会社より研究助成金を受領している者が含まれる。
フェトロージャの感受性(in vitro)
臨床分離グラム陰性菌の分子生物学的性状解析(in vitro)
2件の国際的サーベイランス試験において分離されたグラム陰性菌のうち、カルバペネム耐性の腸内細菌目細菌、緑膿菌、アシネトバクター属を対象に、
フェトロージャの活性を評価した結果、カルバペネマーゼ産生株の96%以上の株がフェトロージャのMIC≦4μg/mLを示しました。
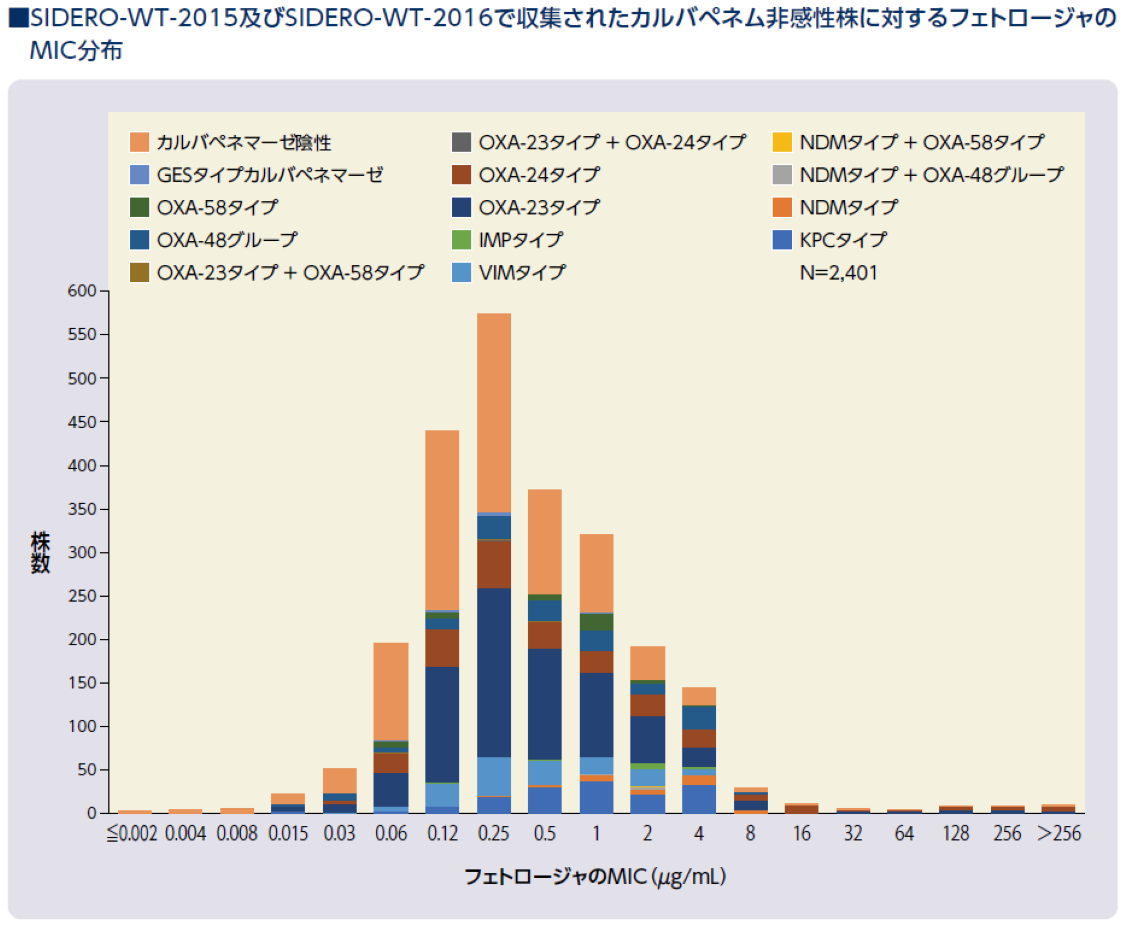
試験方法
SIDERO-WT-2015及びSIDERO-WT-2016の2件の国際的サーベイランス試験において分離されたグラム陰性菌のうち、カルバペネム耐性の腸内細菌目細菌(471株)、
緑膿菌(801株)、アシネトバクター属(1,129株)、計2,401株を対象に、分子生物学的性状解析を実施し、それらに対するフェトロージャの活性を評価した。
社内資料:セフィデロコルの臨床分離グラム陰性菌に対する分子生物学的性状解析
ESCMIDの多剤耐性グラム陰性桿菌感染症治療ガイドライン (欧州集中治療医学会ESICM承認)
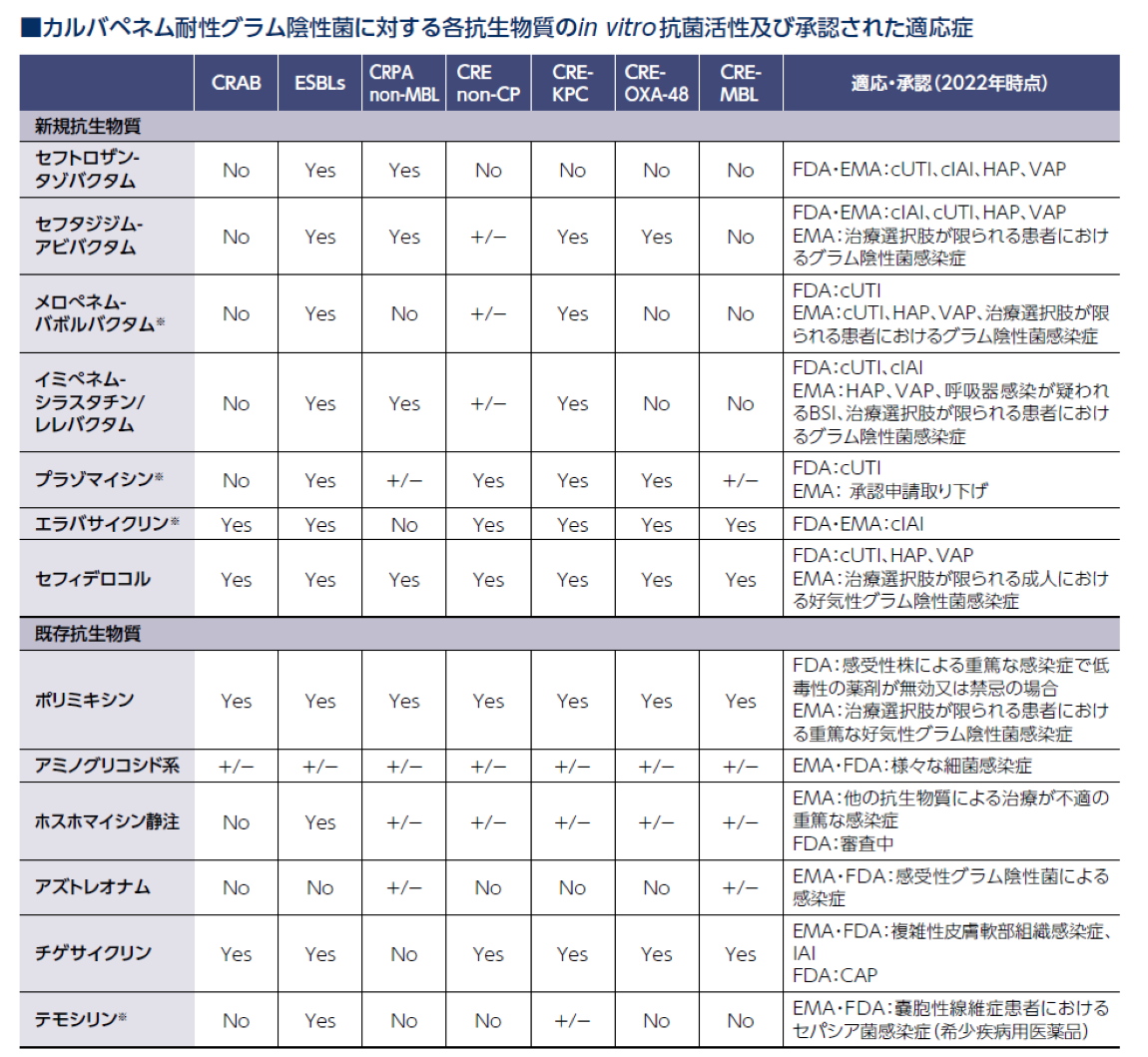
※:本邦未承認
ESCMID: European Society of Clinical Microbiology and Infectious Diseases、欧州臨床微生物感染症学会
CRAB: carbapenem-resistant Acinetobacter baumannii、カルバペネム耐性アシネトバクター・バウマニ
ESBLs: extended-spectrum β-lactmases、基質拡張型β-ラクタマーゼ
CRPA non-MBL: carbapenem-resistant Pseudomonas aeruginosa non metallo-β-lactamase-producing、メタロβ-ラクタマーゼ非産生カルバペネム耐性緑膿菌
CRE non-CP: non-carbapenemase-producing carbapenem-resistant Enterobacterales、カルバペネマーゼ非産生カルバペネム耐性腸内細菌目細菌
MBL : metallo-β-lactamase、メタロβ-ラクタマーゼ
FDA : U.S. Food and Drug Administration、米国食品医薬品局
EMA : European Medicines Agency、欧州医薬品庁
cUTI : complicated urinary tract infections、複雑性尿路感染症
cIAI : complicated intra-abdominal infections、複雑性腹腔内感染症
HAP : hospital-acquired pneumonia、院内肺炎
VAP : ventilator-associated pneumonia、人工呼吸器関連肺炎
CAP : community-acquired pneumonia、市中肺炎
BSI : bloodstream infection、血流感染症
Paul, M. et al.: Clin Microbiol Infect., 2022, 28(4), 521
主なカルバペネム非感性及び多剤耐性グラム陰性桿菌臨床分離株に対する抗菌活性(in vitro)
フェトロージャのブレイクポイントであるMIC≦4μgであったのは、メロペネム非感性腸内細菌目細菌で97.0%、多剤耐性アシネトバクター・バウマニで89.7%、多剤耐性緑膿菌で99.2%でした。多剤耐性ステノトロホモナス・マルトフィリアの結果は以下のグラフのとおりです※1。
※1:試験当時とは異なり、現在ブレイクポイントはMIC1μg /mLに設定されている。
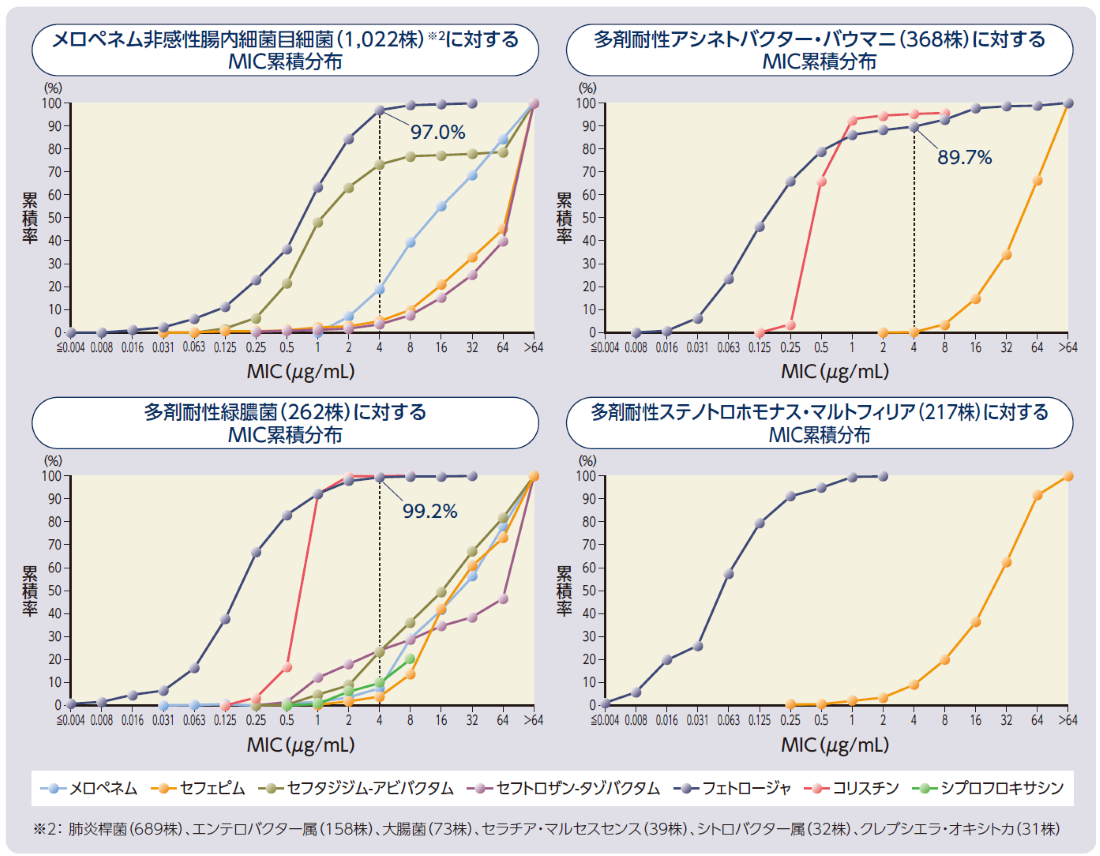
試験方法
2014年~2016年にIHMA(International Health Management Associates, Inc.)が世界52か国から収集した臨床分離株より、カルバペネム非感性及び多剤耐性グラム陰性桿菌1,873株を対象とし、フェトロージャのin vitro抗菌活性を検討した。
臨床分離株の同定には質量分析法(MALDI-TOF)、薬剤感受性試験にはCLSIの微量液体希釈法を用い、 フェトロージャの培地にはID-CAMHBを使用した。
ID-CAMHB: iron-depleted cation-adjusted Mueller Hinton broth、鉄欠乏カチオン調整ミューラーヒントンブロス
Hackel, MA. et al.: Antimicrob Agents Chemother., 2018, 62, e01968より一部改変
本研究は塩野義製薬株式会社の資金により行われた。著者に塩野義製薬株式会社社員が含まれる。
4. 効能・効果
〈適応菌種〉
セフィデロコルに感性の大腸菌、シトロバクター属、肺炎桿菌、クレブシエラ属、エンテロバクター属、セラチア・マルセスセンス、プロテウス属、モルガネラ・モルガニー、緑膿菌、バークホルデリア属、ステノトロホモナス・マルトフィリア、アシネトバクター属
ただし、カルバペネム系抗菌薬に耐性を示す菌株に限る。
〈適応症〉
各種感染症
「警告・禁忌を含む注意事項等情報」等につきましては電子添文情報をご参照ください。
CREDIBLE-CR試験
カルバペネム耐性グラム陰性菌感染症患者を対象とした国際共同第Ⅲ相試験 (CREDIBLE-CR試験)
社内資料:セフィデロコルの第Ⅲ相カルバペネム耐性グラム陰性菌による重症感染症患者を対象とした非盲検試験[承認時評価資料]
Bassetti, M. et al.: Lancet Infect Dis., 2021, 21(2), 226
本研究は塩野義製薬株式会社の資金により行われた。著者に塩野義製薬株式会社社員が含まれる。
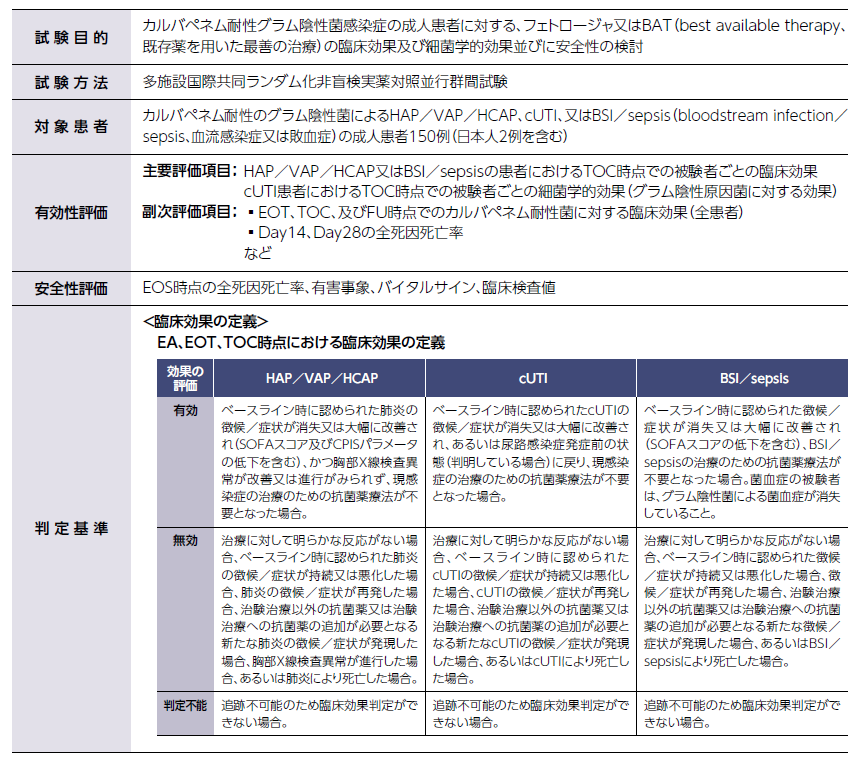
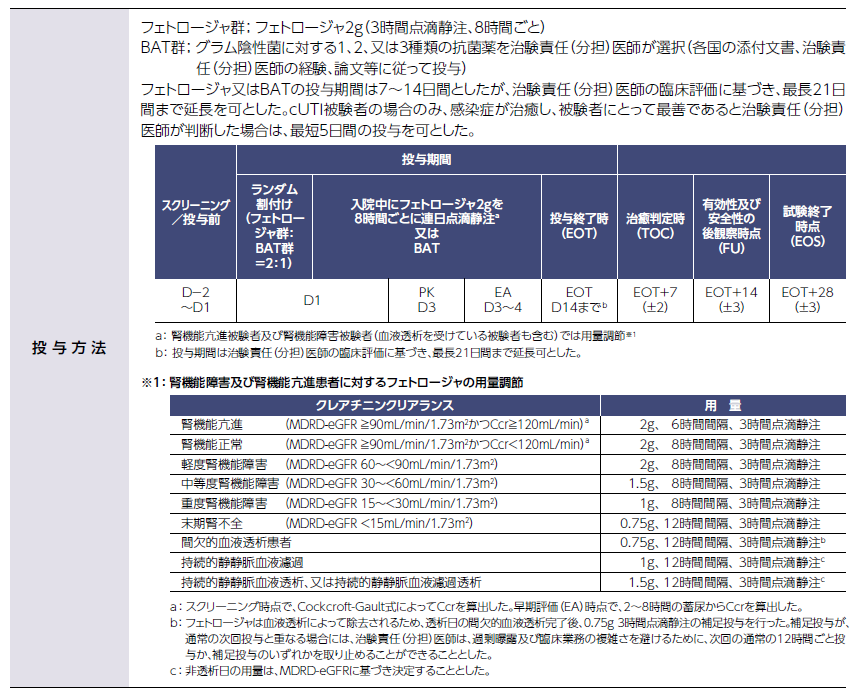
EA: 早期評価時 EOT: 投与終了時 TOC: 治癒判定時 FU: 後観察時 EOS: 試験終了時
7. 用法・用量に関連する注意(一部抜粋)
7.1 腎機能障害のある患者では、以下の基準を目安として用法・用量を調節すること。[9.2、16.6.1 参照]
腎機能障害(Ccr 60mL/min未満)のある又は血液透析を受けている患者※
| Ccr(mL/min)/血液透析患者 | 1回投与量 | 投与間隔 | 投与時間 |
| 30≦Ccr<60 | 1.5g | 8時間毎 | 3時間 |
| 15≦Ccr<30 | 1g | 8時間毎 | 3時間 |
| Ccr<15 | 0.75g | 12時間毎 | 3時間 |
| 血液透析患者 | 0.75g | 12時間毎 | 3時間 |
Ccr:クレアチニンクリアランス
※:血液透析患者では、透析実施後できるだけ速やかに投与すること。
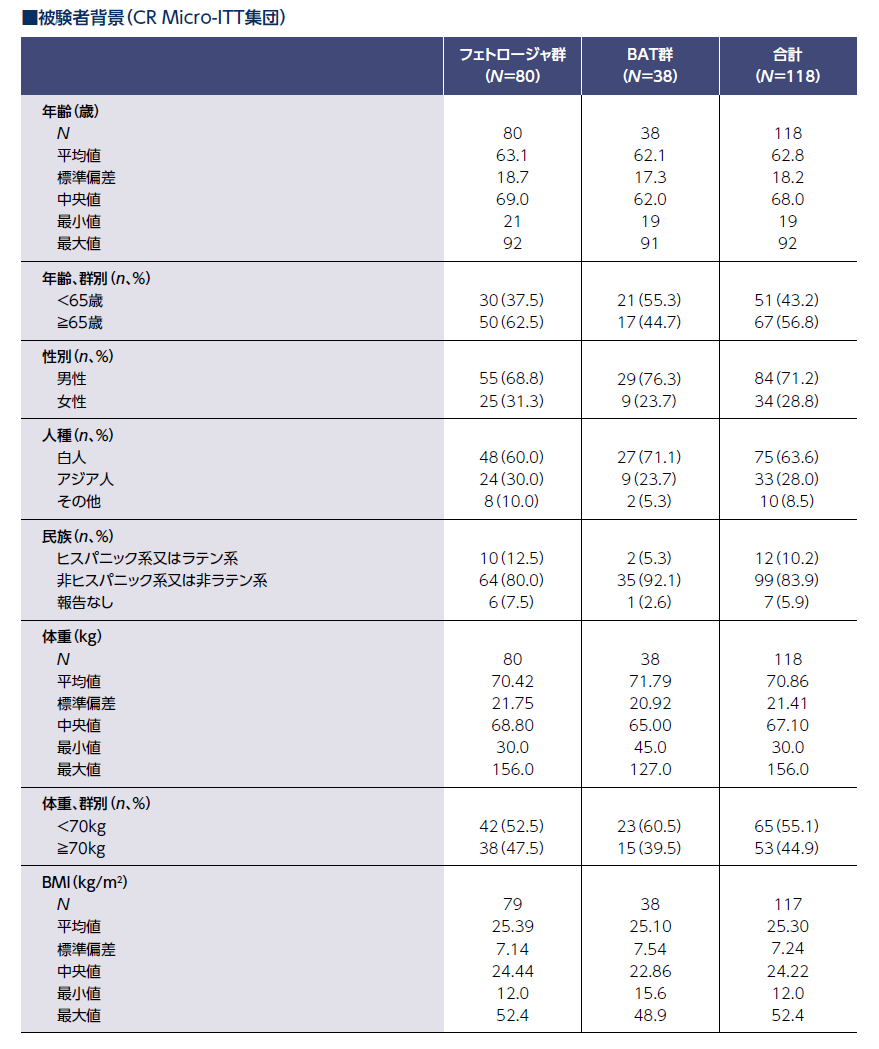
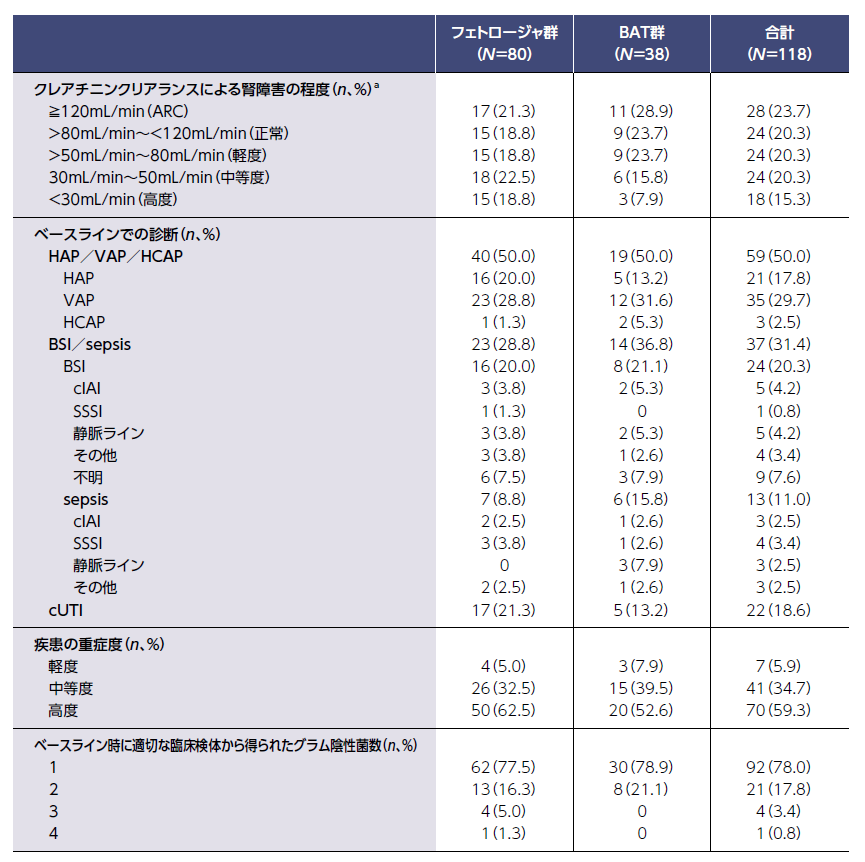
ARC: augmented renal clearance、過大腎クリアランス
cIAI: complicated intra-abdominal infections、複雑性腹腔内感染症
SSSI: skin and skin structure infection、皮膚・軟部組織感染症
a: クレアチニンクリアランスは、中央検査機関から得られたデータに基づき、Cockcroft-Gault式[{(140-年齢(歳))×(体重(kg))}/{72×血清クレアチニン(mg/dL)}、女性の場合は×0.85]を用いて算出した。
治験薬の投与方法
フェトロージャ群は82.5%が単剤投与であったのに対し、BAT群の単剤投与は28.9%でした。
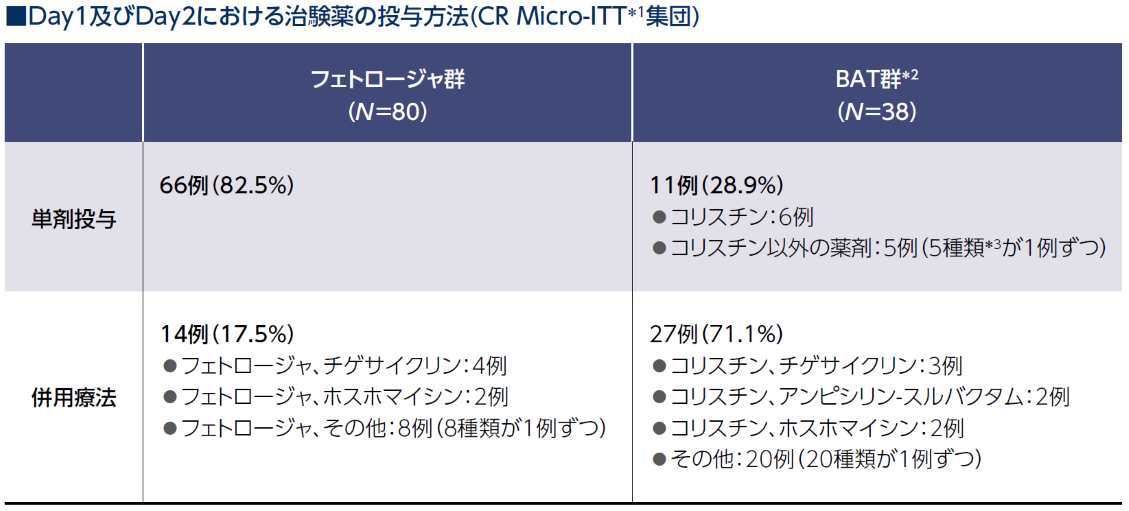
*1 カルバペネム耐性微生物学的Intent-to-treat(集団)
*2 コリスチンに基づいた治療:25例(65.8%)
*3 アミカシン、セフタジジム-アビバクタム、ドリペネム、ホスホマイシン、ゲンタマイシン
投与禁止が行われたケース
フェトロージャ群:1例(フェトロージャ、コリスチン)
フェトロージャ群:1例(フェトロージャ、ゲンタマイシン、チゲサイクリン)
(フェトロージャ群ではコリスチンの投与、3剤投与は禁止されていた)
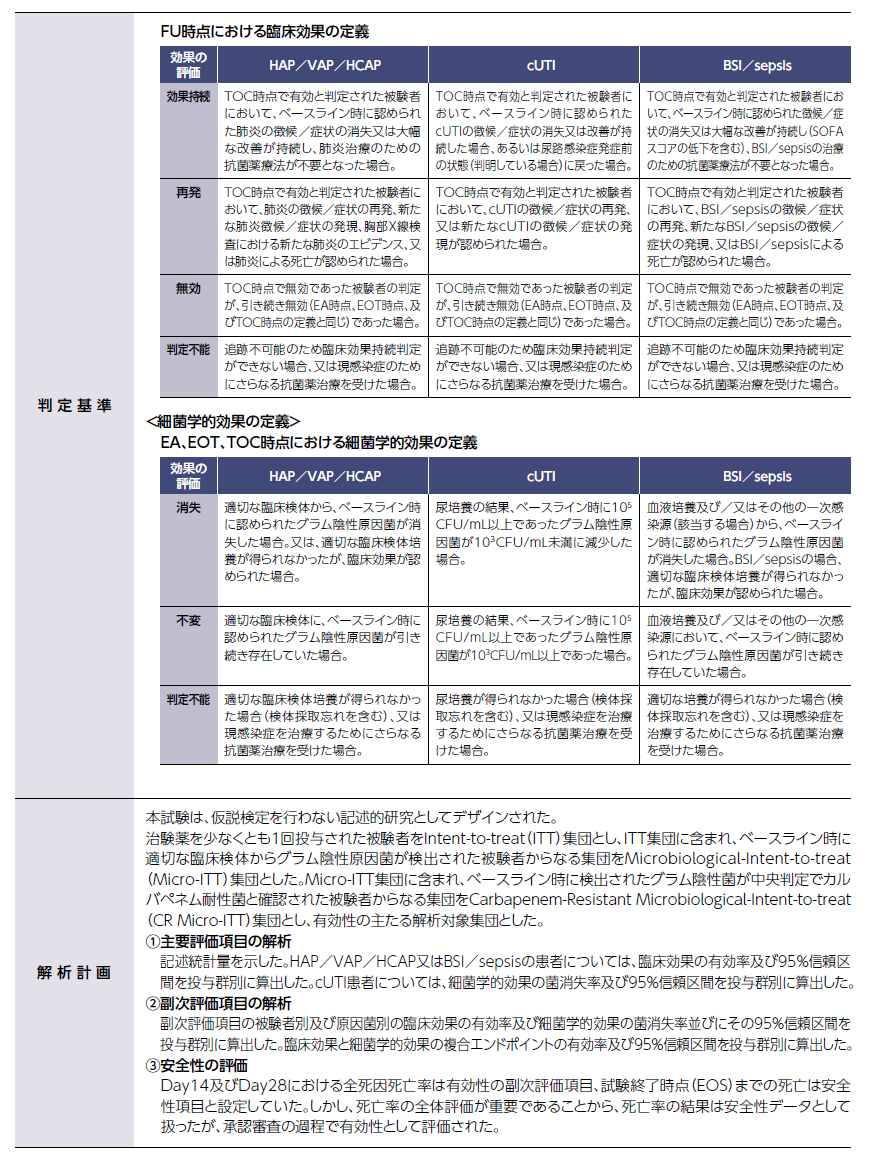
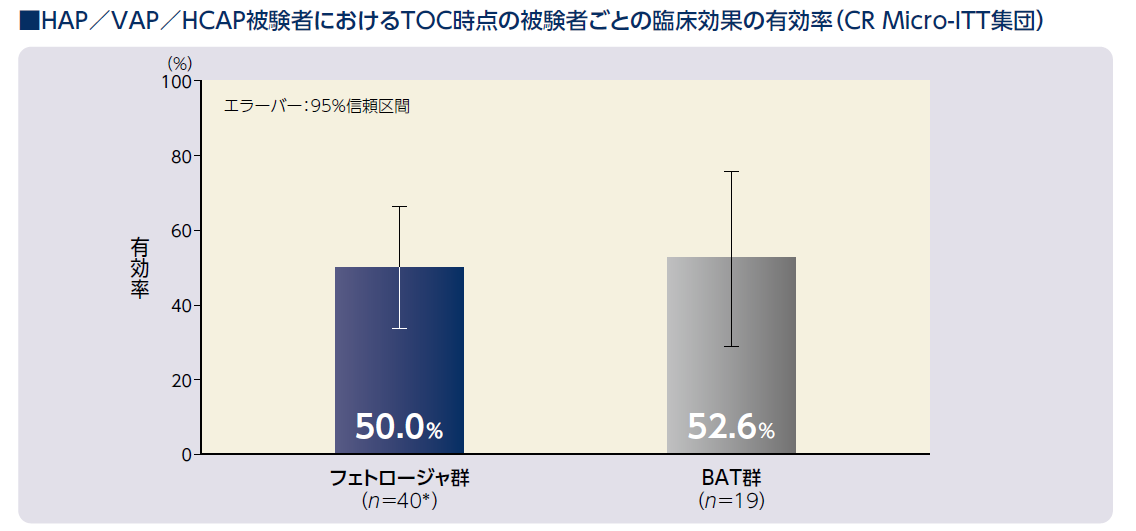
HAP/VAP/HCAP又はBSI/sepsisの患者におけるTOC時点での 被験者ごとの臨床効果(主要評価項目)
HAP/VAP/HCAP被験者におけるTOC時点の被験者ごとの臨床効果の有効率〔95%信頼区間〕は、フェトロージャ群で50.0%(20/40例)〔33.8, 66.2〕、BAT群で52.6%(10/19例)〔28.9, 75.6〕でした。
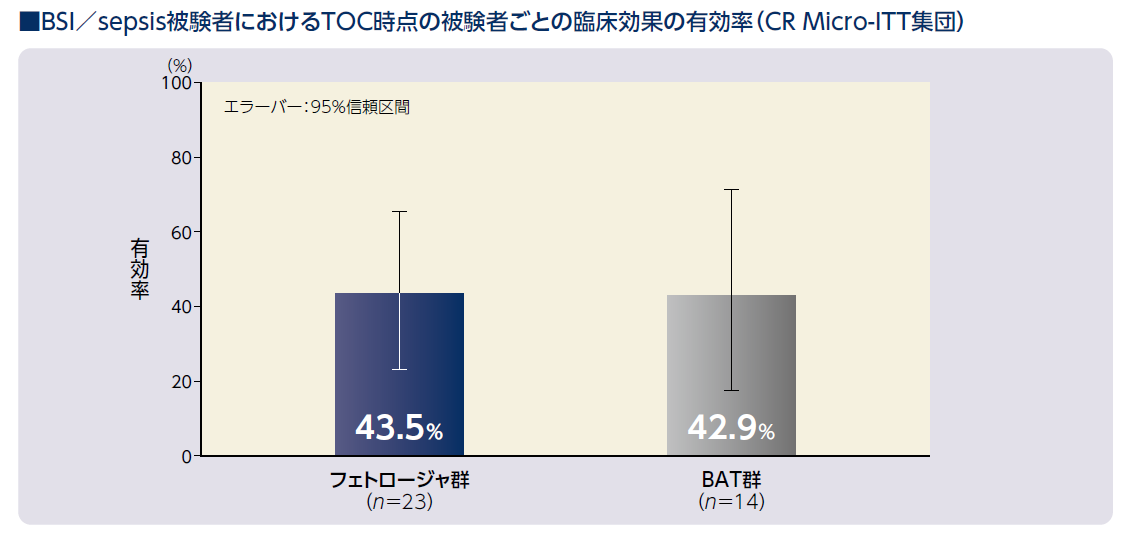
BSI/sepsis被験者におけるTOC時点の被験者ごとの臨床効果の有効率〔95%信頼区間〕は、フェトロージャ群で43.5%(10/23例)〔23.2,65.5〕、BAT群で42.9%(6/14例)〔17.7, 71.1〕でした。
4. 効能・効果
〈適応菌種〉
セフィデロコルに感性の大腸菌、シトロバクター属、肺炎桿菌、クレブシエラ属、エンテロバクター属、セラチア・マルセスセンス、プロテウス属、モルガネラ・モルガニー、緑膿菌、バークホルデリア属、ステノトロホモナス・マルトフィリア、アシネトバクター属
ただし、カルバペネム系抗菌薬に耐性を示す菌株に限る。
〈適応症〉
各種感染症
cUTI患者におけるTOC時点での被験者ごとの細菌学的効果: グラム陰性原因菌に対する効果(主要評価項目)
cUTI被験者におけるTOC時点の被験者ごとの細菌学的効果の菌消失率〔95%信頼区間〕はフェトロージャ群で52.9%(9/17例)〔27.8, 77.0〕、BAT群で1/5例でした。
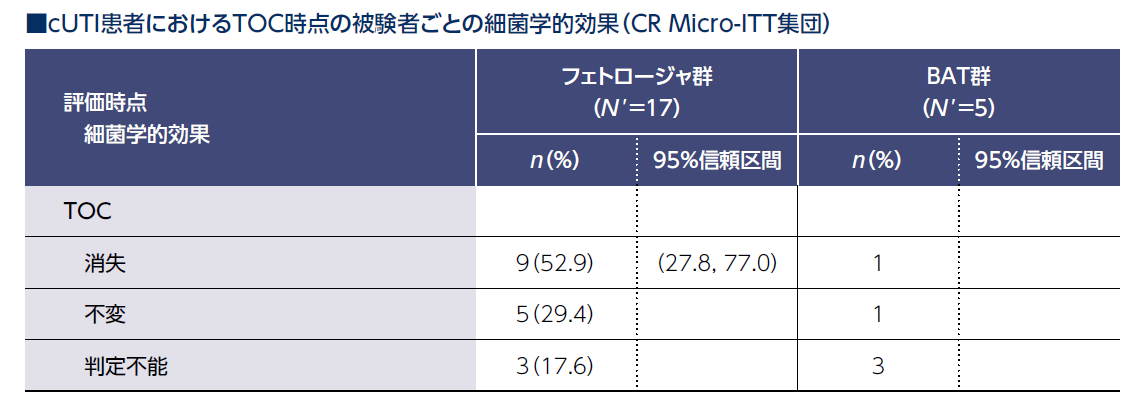
パーセンテージはN' を分母として算出。N' は、特定部位で感染が認められた例数。
EOT、TOC、及びFU時点でのカルバペネム耐性菌に対する臨床効果:全患者 (副次評価項目)
カルバペネム耐性の原因菌別のTOC時点での臨床効果の有効率は、Acinetobacter baumannii ではフェトロージャ群43.2%、BAT群52.9%、Klebsiella pneumoniaeではフェトロージャ群66.7%、BAT群50.0%、Pseudomonas aeruginosaではフェトロージャ群58.3%、BAT群50.0%でした。
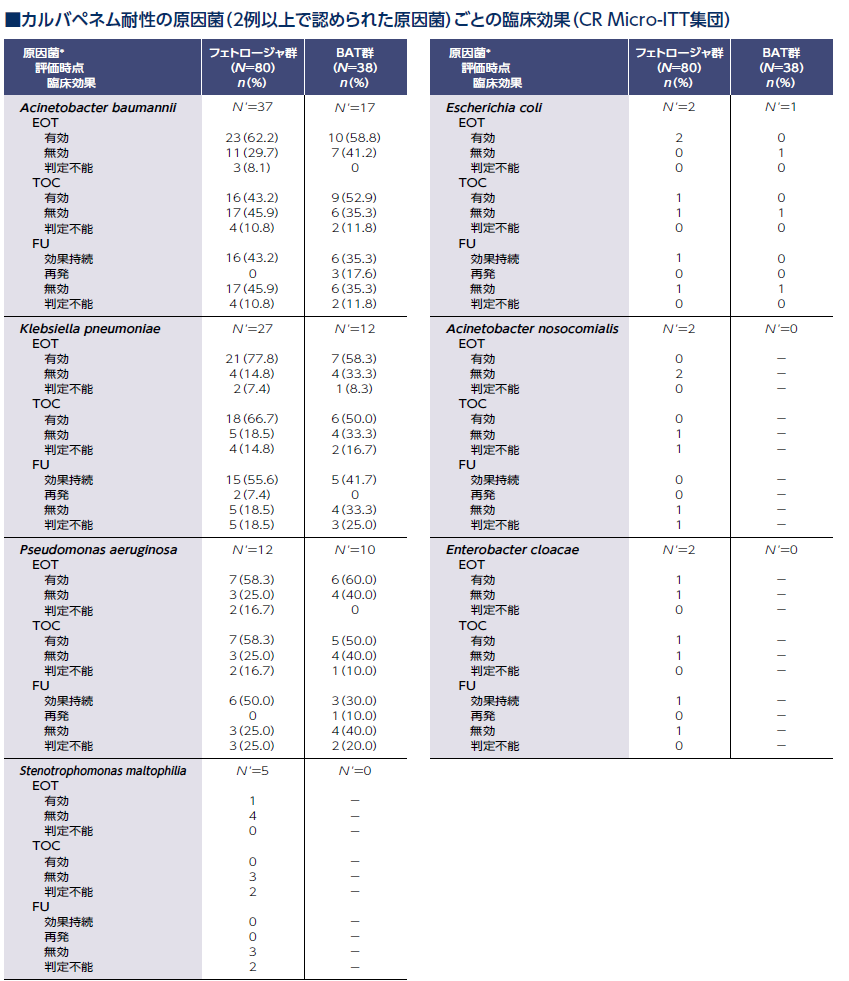
パーセンテージはN' を分母として算出。N' は、原因菌が認められた例数。
*:グラム陰性原因菌は、中央細菌学的検査機関から得られたデータに基づく(入手可能であった場合)。
全死因死亡率(安全性解析対象集団、有効性評価項目)
EOS時点での全死因死亡率は、フェトロージャ群で33.7%(34/101例)、BAT群で18.4%(9/49例)でした※。
※:死亡例のうち、治験責任医師及び治験依頼者により治験薬との因果関係がありと判断された症例は、フェトロージャ群0例、BAT群1例(代謝性アシドーシス、呼吸停止、及び急性腎不全)であった。
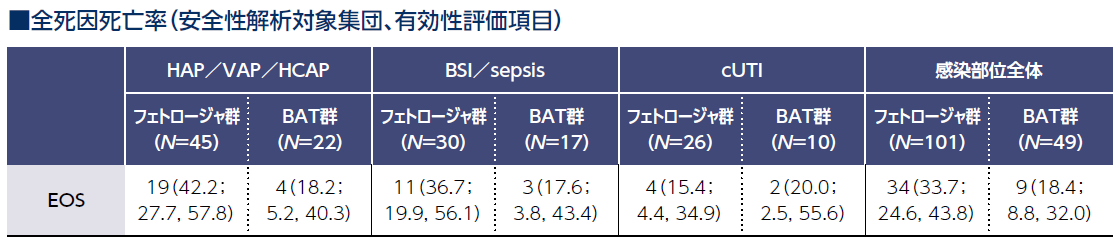
n(%;95%信頼区間)
パーセンテージはNを分母として算出。nは特定の診断を受け、各評価時点で生存状況が確認された安全性解析対象集団の例数。
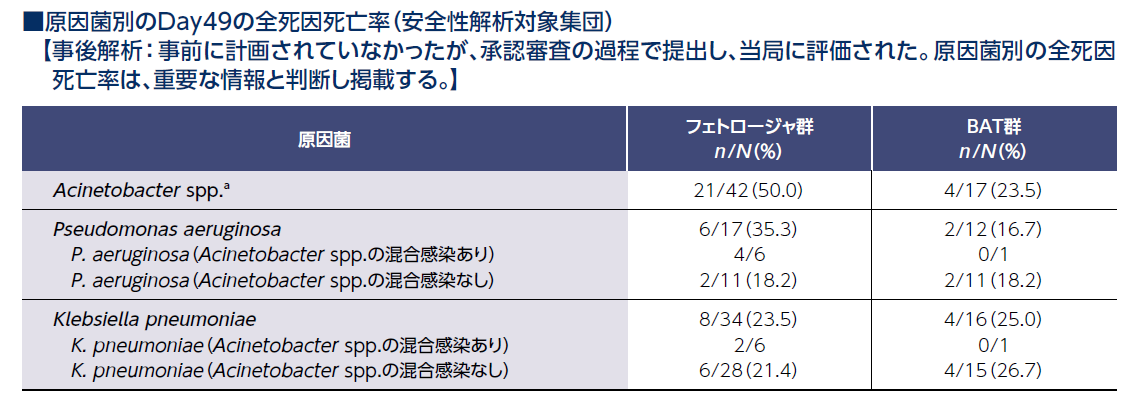
混合感染を考慮し、被験者がAcinetobacter spp.に感染した患者であるか否かを示した。
a: Acinetobacter spp.: A. baumannii、 A. nosocomialis、 A. radioresistens

審査報告書(令和5年11月29日)https://www.pmda.go.jp/drugs/2023/P20231130001/340018000_30500AMX00283_A100_1.pdf
8. 重要な基本的注意(一部抜粋)
8.4 カルバペネム耐性グラム陰性菌による感染症患者を対象とした臨床試験において、原因不明であるものの、本剤が投与されたアシネトバクター属による感染症患者で標準治療群より死亡率が高い傾向が認められた。本剤の使用にあたっては他の治療法も考慮のうえ、本剤を使用する場合は、患者の状 態を慎重に
観察すること。[17.1.1参照]
安全性
カルバペネム耐性グラム陰性菌感染症患者を対象とした国際共同第Ⅲ相試験において、フェトロージャ群の副作用発現率は14.9%、BAT群は22.4%でした。
重篤な副作用は、フェトロージャ群で1例(トランスアミナーゼ上昇)、BAT群で5例(てんかん重積状態、アナフィラキシー反応、急性腎不全、敗血症性ショック、代謝性アシドーシス、呼吸停止及び急性腎不全各1例)でした。
投与中止に至った副作用はフェトロージャ群で3例(発熱、トランスアミナーゼ上昇、薬疹各1例)、BAT群で2例(アナフィラキシー反応、てんかん重積状態各1例)でした。
本試験において死亡に至った副作用は、フェトロージャ群では認められず、BAT群で1例(代謝性アシドーシス、呼吸停止及び急性腎不全)でした。
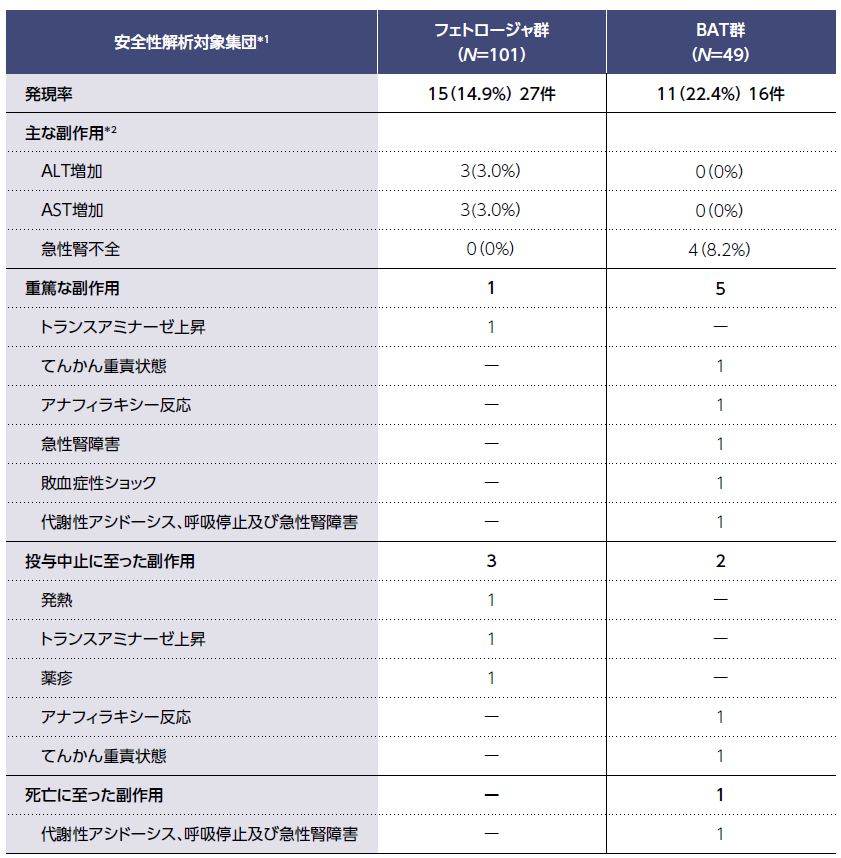
*1: ランダム割付けされ、治験薬が少なくとも1回投与されたすべての被験者
*2: いずれかの投与群で3例以上に発現
References
1) CDC プレスリリース 2013年3月
https://archive.cdc.gov/#/details?url=https://www.cdc.gov/media/releases/2013/p0305_deadly_bacteria.html
2) ANTIBIOTIC RESISTANCE THREATS in the United States, 2013
3) THE REVIEW ON ANTIMICROBIAL RESISTANCE CHAIRED BY JIM O’NEILL: TACKLING DRUG-RESISTANT INFECTIONS GLOBALLY: AN OVERVIEW
OF OUR WORK, 2016
4) WHO Bacterial Priority Pathogens List, 2024
https://iris.who.int/bitstream/handle/10665/376776/9789240093461-eng.pdf
